Hvilket element opfører sig kemisk ligner natrium?
Her er hvorfor:
* De er begge i den samme gruppe (gruppe 1, alkalimetaller) af den periodiske tabel. Dette betyder, at de har det samme antal valenselektroner (1) og derfor lignende kemiske egenskaber.
* de danner let +1 ioner. Både natrium og kalium mister en elektron for at opnå en stabil elektronkonfiguration.
* de er meget reaktive metaller. De reagerer kraftigt med vand og luft og frigiver brintgas.
Mens andre elementer i gruppe 1 også vil have lignende egenskaber som natrium, er kalium det tætteste med hensyn til reaktivitet og adfærd.
Sidste artikelHvad sker der, når kobber reagerer med HCL?
Næste artikelHvad er oxidationstilstanden i gruppe 13?
 Varme artikler
Varme artikler
-
 Selvhelbredende omvendt filter åbner døren for mange nye anvendelserSelvhelbredende omvendt filter tillader store partikler igennem, men udelukker mindre partikler og gasser. Kredit:Tak-Sing Wong/Birgitt Boschitsch, Penn State En selvhelbredende membran, der funge
Selvhelbredende omvendt filter åbner døren for mange nye anvendelserSelvhelbredende omvendt filter tillader store partikler igennem, men udelukker mindre partikler og gasser. Kredit:Tak-Sing Wong/Birgitt Boschitsch, Penn State En selvhelbredende membran, der funge -
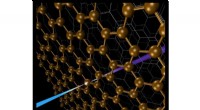 Ny sonde til hemmelighederne ved komplekse grænsefladerForskere har udtænkt en spektroskopi-metode - baseret på blød røntgen-anden-harmonisk generation - der sonderer begravede grafenlag inde i grafit. Kredit:US Department of Energy I genopladelige ba
Ny sonde til hemmelighederne ved komplekse grænsefladerForskere har udtænkt en spektroskopi-metode - baseret på blød røntgen-anden-harmonisk generation - der sonderer begravede grafenlag inde i grafit. Kredit:US Department of Energy I genopladelige ba -
 Ny teknologi til fremstilling af porøst aluminiumDen nye teknologi til fremstilling af usænkeligt materiale fra aluminiumslegeringen blev patenteret ved Peter the Great St. Petersburg Polytechnic University (SPbPU). Kredit:Peter den Store St. Peters
Ny teknologi til fremstilling af porøst aluminiumDen nye teknologi til fremstilling af usænkeligt materiale fra aluminiumslegeringen blev patenteret ved Peter the Great St. Petersburg Polytechnic University (SPbPU). Kredit:Peter den Store St. Peters -
 Forskere foreslår, at man anvender metanoverflader af guld til at bestemme stoffets molekylære sam…Guldpartikler Kredit:Dmitry Bayer En ny metode vil gøre det muligt at skabe kompakte enheder, der nøjagtigt bestemmer den molekylære sammensætning af en væske eller gas, og hjælpe med at identific
Forskere foreslår, at man anvender metanoverflader af guld til at bestemme stoffets molekylære sam…Guldpartikler Kredit:Dmitry Bayer En ny metode vil gøre det muligt at skabe kompakte enheder, der nøjagtigt bestemmer den molekylære sammensætning af en væske eller gas, og hjælpe med at identific
- Hvad sker der med en væske, når de frigiver nok energi?
- Gamle skelet afslører amputationsoperation for 31.000 år siden
- Hvordan laves vulkansk aske?
- Hvad betyder udtrykket solar?
- Hvordan en biofysisk simuleringsmetode kan fremskynde opdagelsen af lægemiddelmål
- Er den videnskabelige undersøgelse af distributionselektromagnetiske bølger med energi, og hvordan…


