Hvornår betragtes en kemisk ligning som afbalanceret?
* Antallet af atomer i hvert element på reaktanternes side (venstre side) af ligningen er lig med antallet af atomer i det samme element på produkternes side (højre side) af ligningen.
I enklere termer:
* Du har det samme antal af hver type atom før og efter den kemiske reaktion.
Dette er baseret på lov om bevarelse af masse , der siger, at masse ikke kan skabes eller ødelægges i almindelige kemiske reaktioner.
For eksempel:
Ubalanceret ligning:
H₂ + O₂ → H₂O
afbalanceret ligning:
2H₂ + O₂ → 2H₂O
I dette eksempel har vi:
* reaktanter: 2 hydrogenatomer (H₂) og 2 iltatomer (O₂)
* Produkter: 4 Hydrogenatomer (2H₂) og 2 iltatomer (2O₂)
Den afbalancerede ligning har nu det samme antal af hver type atom på begge sider.
Sidste artikelDonerer eller accepterer natrium en elektron?
Næste artikelHvad er hårdheden af pyroxen?
 Varme artikler
Varme artikler
-
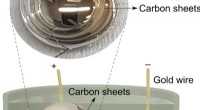 Flydende metaller nedbryder organiske brændstoffer til ultratynde grafitpladerKredit:University of New South Wales For første gang, forskere ved University of New South Wales (UNSW), Sydney, Australien, har demonstreret syntesen af ultratynde grafitiske materialer ved stu
Flydende metaller nedbryder organiske brændstoffer til ultratynde grafitpladerKredit:University of New South Wales For første gang, forskere ved University of New South Wales (UNSW), Sydney, Australien, har demonstreret syntesen af ultratynde grafitiske materialer ved stu -
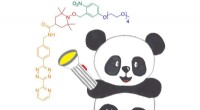 En ny proteinspin-mærkningsteknikDet nye fotoaktiverbare nitroxid til DAinv reaktionsspinmærke for proteiner, PanDA. Det kan ligeres til proteiner gennem en DAinv cycloaddition til genetisk kodede ikke-kanoniske aminosyrer. Kredit:An
En ny proteinspin-mærkningsteknikDet nye fotoaktiverbare nitroxid til DAinv reaktionsspinmærke for proteiner, PanDA. Det kan ligeres til proteiner gennem en DAinv cycloaddition til genetisk kodede ikke-kanoniske aminosyrer. Kredit:An -
 Forskere løser en materialemysternøgle til næste generations elektroniske enhederMaterialevidenskab og teknik postdoktorforsker Hyungwoo Lee kigger inde i et tyndfilmsdepositionssystem under vækst af oxid tyndfilmstruktur. Kredit:Renee Meiller Lennon og McCartney. Abbott og Co
Forskere løser en materialemysternøgle til næste generations elektroniske enhederMaterialevidenskab og teknik postdoktorforsker Hyungwoo Lee kigger inde i et tyndfilmsdepositionssystem under vækst af oxid tyndfilmstruktur. Kredit:Renee Meiller Lennon og McCartney. Abbott og Co -
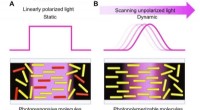 Fotopolymerisationsudløst molekylær bevægelse til fleksibelt flydende krystaldisplayA repræsenterer den molekylære justering gennem konventionelle fotojusteringsmetoder. B repræsenterer den molekylære justering opnået gennem den aktuelt rapporterede scanningsbølgefotopolymeriseringsm
Fotopolymerisationsudløst molekylær bevægelse til fleksibelt flydende krystaldisplayA repræsenterer den molekylære justering gennem konventionelle fotojusteringsmetoder. B repræsenterer den molekylære justering opnået gennem den aktuelt rapporterede scanningsbølgefotopolymeriseringsm
- Gennembrud i tynde elektrisk ledende ark baner vej for mindre elektroniske enheder
- Nyt regime i Casimir-styrken observeret
- Hvad hedder Jordens drejning?
- Nyfødte insekter fanget i rav viser det første bevis på, hvordan man knækker et æg
- Hvad er frekvensen, når 300 bølger passerer et punkt på et minut?
- Er skorpen dannet eller ødelagt ved glidende grænse?


