Hvad er farven på vandig brom efter tilsætning af carbonhydrid?
Her er hvorfor:
* brom (Br2) I vand er en rødbrun løsning.
* Når der tilsættes et carbonhydrid, reagerer bromen med det i en halogeneringsreaktion . Denne reaktion involverer typisk tilsætning af brom på tværs af en dobbelt- eller tredobbelt binding i carbonhydridet.
* Produktet af denne reaktion er en bromeret carbonhydrid , som normalt er farveløs.
* Når bromen reagerer med kulbrinteren, falder den orangebrune farve på bromopløsningen og forsvinder til sidst, hvilket efterlader en farveløs opløsning.
Vigtig note: Denne farveændring er en almindelig indikation af tilstedeværelsen af et umættet carbonhydrid (en med dobbelt- eller tredobbelt bindinger). Det er dog ikke en endelig test for umættelse, da nogle andre reaktioner også kan forbruge brom.
Sidste artikelBrinell -hårdhed på 300HB i PSI og MPA?
Næste artikelHvad er udseendet af en metal- og kulstofkombination?
 Varme artikler
Varme artikler
-
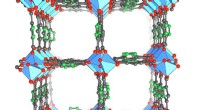 I ørkenforsøg, næste generations vandopsamler leverer frisk vand fra luftenKrystalstrukturen af de nyeste, aluminiumsbaseret metal-organisk ramme, MOF-303, som fanger dobbelt så meget vand som den tidligere MOF, der blev brugt i vandhøsteren. Kredit:Yaghi lab, UC Berkeley
I ørkenforsøg, næste generations vandopsamler leverer frisk vand fra luftenKrystalstrukturen af de nyeste, aluminiumsbaseret metal-organisk ramme, MOF-303, som fanger dobbelt så meget vand som den tidligere MOF, der blev brugt i vandhøsteren. Kredit:Yaghi lab, UC Berkeley -
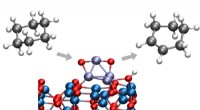 Forskere er banebrydende for den nye kemiske konverteringsproces ved lav temperaturArgonne -kemikere har identificeret en måde at konvertere cyclohexan til cyclohexen eller cyclohexadien, begge vigtige kemikalier i en lang række industrielle processer. Den nye proces finder sted ved
Forskere er banebrydende for den nye kemiske konverteringsproces ved lav temperaturArgonne -kemikere har identificeret en måde at konvertere cyclohexan til cyclohexen eller cyclohexadien, begge vigtige kemikalier i en lang række industrielle processer. Den nye proces finder sted ved -
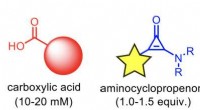 Lysinduceret modifikation af en carboxylsyre med en aminocyclopropenonFotoudløst modifikation af en carboxylsyre ved hjælp af en aminocyclopropenon. Reaktionen afsluttes på kort tid (5-10 min) selv ved lav koncentration (10-20 mM). Modifikationsreaktionen forløber i op
Lysinduceret modifikation af en carboxylsyre med en aminocyclopropenonFotoudløst modifikation af en carboxylsyre ved hjælp af en aminocyclopropenon. Reaktionen afsluttes på kort tid (5-10 min) selv ved lav koncentration (10-20 mM). Modifikationsreaktionen forløber i op -
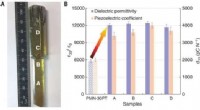 Forskere finder, at tilføjelse af sjældne jordarters element til piezoelektriske krystaller forbed…Billede og elektromekaniske egenskaber af [001]-orienterede Sm-doterede PMN-PT-krystaller. (A) Billede af Sm-PMN-PT-krystal som vokset. Sammensætningen af punkt A, B, C, og D er anført i tabel S1. (
Forskere finder, at tilføjelse af sjældne jordarters element til piezoelektriske krystaller forbed…Billede og elektromekaniske egenskaber af [001]-orienterede Sm-doterede PMN-PT-krystaller. (A) Billede af Sm-PMN-PT-krystal som vokset. Sammensætningen af punkt A, B, C, og D er anført i tabel S1. (
- Hvilke fire næringsstoffer findes i plasma?
- Stigende vejafgifter fra monsunoversvømmelser hæmmer Sydasien-virusindsatsen
- Hvad er tre slags stof, der udfører varme dårligt?
- Formede solen uden for roterende interstelear sky?
- Hvad er nogle eksempler på materiale, der tillader elektricitet at flyde?
- At se lyset:Forskere kombinerer teknologier for bedre lysstyring


