Hvad er krystalstrukturen af nitrogen?
Derfor har nitrogen ikke en traditionel krystalstruktur, som faste stoffer gør. Her er hvorfor:
* gasformig tilstand: Ved normale forhold er nitrogenmolekyler vidt placeret og konstant bevægende, hvilket gør det umuligt for dem at danne en stiv, ordnet struktur.
* svage intermolekylære kræfter: De kræfter, der holder nitrogenmolekyler sammen (van der Waals -kræfter), er meget svage. Disse kræfter er ikke stærke nok til at skabe et krystallinsk gitter.
Imidlertid kan nitrogen imidlertid eksistere i forskellige faste faser med specifikke krystalstrukturer under ekstreme forhold i forskellige faser med specifikke krystalstrukturer:
* alfa nitrogen (α-N 2 ): Dette er den mest stabile faste fase af nitrogen, opnået ved højt tryk (over 3,5 GPa) og lav temperatur (under 35,6 K). Det har en hexagonal tætpakket (HCP) struktur.
* beta nitrogen (ß-n 2 ): Denne fase dannes ved højere temperaturer (35,6-44,5 K) og lidt højere tryk (4,5 GPa). Det har en kubisk tætpakket (CCP) struktur.
* gamma nitrogen (γ-N 2 ): Denne fase forekommer ved endnu højere temperaturer (44,5-63 K) og tryk (ca. 6 GPa). Det har en rhombohedral struktur.
* Andre faser: Flere andre højtryksfaser af fast nitrogen er blevet opdaget, hver med sin egen unikke krystalstruktur.
Selvom nitrogen typisk er en gas og ikke har en konventionel krystalstruktur, kan det udvise forskellige krystallinske strukturer under højt tryk og lav temperatur.
Sidste artikelHvor mange elektroner optager p orbitaler i et bromatom?
Næste artikelHvad forårsager en brintbinding?
 Varme artikler
Varme artikler
-
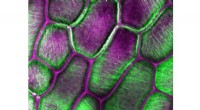 Nye cellulosefund kan føre til nye kemikalier, biobrændstofferForskere afslørede den snoede krystalorientering af cellulosefibre, afbilledet her i grønt i cellerne i en løgskal. Kredit:Edward Wagner, Cosgrove Lab, Penn State En multiinstitutionel forskergrup
Nye cellulosefund kan føre til nye kemikalier, biobrændstofferForskere afslørede den snoede krystalorientering af cellulosefibre, afbilledet her i grønt i cellerne i en løgskal. Kredit:Edward Wagner, Cosgrove Lab, Penn State En multiinstitutionel forskergrup -
 Forskeres beregningsmetoder baner vejen for næste generations membranteknologi til vandrensningKonceptillustration af en vandrensningsmembran med beregningsmæssigt designet, molekylær skala mønstre af overfladefunktionelle grupper, som tilsammen fungerer til at afvise en række forskellige molek
Forskeres beregningsmetoder baner vejen for næste generations membranteknologi til vandrensningKonceptillustration af en vandrensningsmembran med beregningsmæssigt designet, molekylær skala mønstre af overfladefunktionelle grupper, som tilsammen fungerer til at afvise en række forskellige molek -
 Hurtige og pålidelige tests for legionellabakterier i vandKredit:Giovanni Cancemi, Shutterstock En fuldautomatisk testanordning kan nu installeres på vandsteder, der er mistænkt for forurening med legionella-bakterier. Enheden lover mere pålidelige resul
Hurtige og pålidelige tests for legionellabakterier i vandKredit:Giovanni Cancemi, Shutterstock En fuldautomatisk testanordning kan nu installeres på vandsteder, der er mistænkt for forurening med legionella-bakterier. Enheden lover mere pålidelige resul -
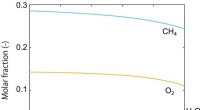 Ydeevne af methankonverteringsfast katalysator forudsiges ved teoretisk beregningFigur 1. Molfraktionsændring Molfraktion langs reaktionstiden (-erne) beregnet ved reaktorsimuleringen. Indløbsgassen bestod af CH4, O2, og He (som inert gas). Det samlede tryk blev sat til P =1 bar,
Ydeevne af methankonverteringsfast katalysator forudsiges ved teoretisk beregningFigur 1. Molfraktionsændring Molfraktion langs reaktionstiden (-erne) beregnet ved reaktorsimuleringen. Indløbsgassen bestod af CH4, O2, og He (som inert gas). Det samlede tryk blev sat til P =1 bar,
- Hvilke gramnegative bakterier vokser ikke på macconkey og EMB?
- Hvordan bruger folk vandkraft energi?
- A (n) er et hul i den geologiske rekord, hvor nogle klippelag er gået tabt på grund af erosion.?
- Kraftige skovbrande komplicerer naturlig regenerering for californiske nåletræer
- Hvad er tætheden af et objekt, der har en masse 25g og bind 10 cm t tredje effekt?
- Undersøgelse viser, hvordan klimaændringer truer sundheden


