En fortyndet vandig kaliumnitratopløsning klassificeres bedst som en?
* elektrolytter er stoffer, der udfører elektricitet, når de opløses i vand. Dette sker, fordi de adskiller sig i ioner (ladede partikler), når de er i opløsning.
* kaliumnitrat (KNO3) er en ionisk forbindelse. Når det opløses i vand, bryder det fra hinanden i kaliumioner (K+) og nitrationer (NO3-). Disse ioner kan frit flytte, hvilket giver løsningen til at udføre elektricitet.
Lad os nedbryde, hvorfor andre muligheder ikke er den bedste pasform:
* nonelectrolyte: Disse stoffer adskiller sig ikke i ioner, når de opløses i vand, så de kan ikke udføre elektricitet. Eksempler inkluderer sukker og ethanol.
* kolloid: Kolloider er blandinger, hvor partikler spredes i et medium. De kan være uigennemsigtige eller gennemskinnelige, men partiklerne er store nok til at sprede lys. Kaliumnitratopløsning er gennemsigtig og udviser ikke denne spredning.
* Suspension: Suspensioner er blandinger, hvor partikler er store nok til at slå sig ud over tid. Kaliumnitrat opløses fuldstændigt i vand og danner ikke en suspension.
Kortfattet: En fortyndet vandig kaliumnitratopløsning er en elektrolyt på grund af tilstedeværelsen af ioner, der dannes, når saltet opløses.
Sidste artikelEr det let eller svært at finde hydrogenperoxid?
Næste artikelHvad hedder Compound HCI?
 Varme artikler
Varme artikler
-
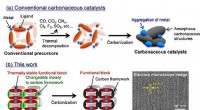 En ny synteserute for alternative katalysatorer af ædelmetallerSynteseskemaer af (a) konventionelle carbonholdige katalysatorer og (b) dette arbejde for ordnede carbonholdige rammer. Kredit:Hirotomo Nishihara Forskere har udviklet en ny synteserute for altern
En ny synteserute for alternative katalysatorer af ædelmetallerSynteseskemaer af (a) konventionelle carbonholdige katalysatorer og (b) dette arbejde for ordnede carbonholdige rammer. Kredit:Hirotomo Nishihara Forskere har udviklet en ny synteserute for altern -
 Bio-sensing kontaktlinse kunne en dag måle blodsukker, andre kropsfunktionerGennemsigtige biosensorer i kontaktlinser - gjort synlige i denne kunstners gengivelse - kunne snart hjælpe med at spore vores helbred. Kredit:Jack Forkey/Oregon State University Gennemsigtige bio
Bio-sensing kontaktlinse kunne en dag måle blodsukker, andre kropsfunktionerGennemsigtige biosensorer i kontaktlinser - gjort synlige i denne kunstners gengivelse - kunne snart hjælpe med at spore vores helbred. Kredit:Jack Forkey/Oregon State University Gennemsigtige bio -
 Nyt superomnifobisk glas svæver højt på sommerfuglevingerne ved hjælp af maskinlæringKredit:CC0 Public Domain Glas til teknologier som displays, tabletter, bærbare computere, smartphones, og solceller skal passere lys igennem, men kunne drage fordel af en overflade, der afviser va
Nyt superomnifobisk glas svæver højt på sommerfuglevingerne ved hjælp af maskinlæringKredit:CC0 Public Domain Glas til teknologier som displays, tabletter, bærbare computere, smartphones, og solceller skal passere lys igennem, men kunne drage fordel af en overflade, der afviser va -
 Går med DNA-strømmen:Livets molekyle finder nye anvendelser i mikroelektronikForskere ved Arizona State University, i samarbejde med NYU og Duke University, har for nylig designet, skabt og testet et DNA-kredsløb, der er i stand til at opdele og kombinere strøm, meget som en a
Går med DNA-strømmen:Livets molekyle finder nye anvendelser i mikroelektronikForskere ved Arizona State University, i samarbejde med NYU og Duke University, har for nylig designet, skabt og testet et DNA-kredsløb, der er i stand til at opdele og kombinere strøm, meget som en a
- Billede:OSIRIS-REx ser Jorden under forbiflyvning
- Hvilken planet har den sjette største satellit i solsystemet?
- Hvordan påvirkes bevægelse af magt?
- Den diskrete-tidsfysik gemmer sig inde i vores kontinuerte tidsverden
- Når et gen kontrollerer to eller flere fænotypiske træk?
- Når man ser på månen og ser en voksende halvmåne fra Jorden, hvorfor står hele side af det over…


