Benzin og vand blandes ikke hvorfor?
* Polaritet: Vand er en polar molekyle. Dette betyder, at dens elektroner er ujævnt fordelt, hvilket skaber en lidt positiv ende og en lidt negativ ende. Dette gør det muligt for vandmolekyler at danne stærke brintbindinger med hinanden.
* ikke -polaritet: Benzin er på den anden side en ikke -polær Blanding af kulbrinter. Disse molekyler har en jævn fordeling af elektroner og har ikke den samme tiltrækning til hinanden som vandmolekyler gør.
hvorfor de ikke blander:
1. Intermolekylære kræfter: De stærke hydrogenbindinger mellem vandmolekyler er meget stærkere end de svagere van der Waals -kræfter mellem benzinmolekyler.
2. "som opløser som": Polære stoffer (som vand) har en tendens til at opløse andre polære stoffer. Ikke -polære stoffer (som benzin) har en tendens til at opløse andre ikke -polære stoffer. Da vand og benzin har meget forskellige polariteter, afviser de hinanden.
Forestil dig dette: Tænk på vand som en gruppe mennesker, der holder hænder, danner en stram cirkel. Benzinmolekyler er som individer, der foretrækker at være af sig selv. Vandmolekylerne lader ikke benzinmolekylerne tilslutte sig deres cirkel, så de to stoffer forbliver adskilte.
Sidste artikelHvad er forskellen mellem sulfat og sulfitter?
Næste artikelOpløselighed af KCl ved 100 grader C?
 Varme artikler
Varme artikler
-
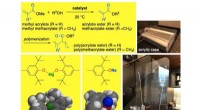 Industriel forbindelse får en miljøvenlig reaktionNatrium- eller magnesiumaryloxider kan katalysere transesterificeringen af methyl(meth)acrylat ved stuetemperatur, med høj kemoselektivitet, producerer et højt udbytte af (meth) acrylatester, og ude
Industriel forbindelse får en miljøvenlig reaktionNatrium- eller magnesiumaryloxider kan katalysere transesterificeringen af methyl(meth)acrylat ved stuetemperatur, med høj kemoselektivitet, producerer et højt udbytte af (meth) acrylatester, og ude -
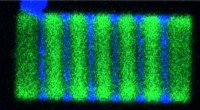 Ny klasse af bløde halvledere kunne transformere HD-skærmeEn 2-D plade, der viser skiftevis cæsium blychlorid (blå) og cæsium blybromid (grøn) segmenter. Kredit:Letian Dou/Berkeley Lab og Connor G. Bischak/UC Berkeley En ny type halvleder kan være på vej
Ny klasse af bløde halvledere kunne transformere HD-skærmeEn 2-D plade, der viser skiftevis cæsium blychlorid (blå) og cæsium blybromid (grøn) segmenter. Kredit:Letian Dou/Berkeley Lab og Connor G. Bischak/UC Berkeley En ny type halvleder kan være på vej -
 Bedre forståelse af principperne for siliciumætsning fører til forbedret overflademønsterVed hjælp af nøje udvalgte kombinationer af metaller, det er muligt at etse indviklede mønstre på en siliciumoverflade, som vist ovenfor. Kredit:Ref. 1 og licenseret under CC BY 4.0 © 2016 L. Kong et
Bedre forståelse af principperne for siliciumætsning fører til forbedret overflademønsterVed hjælp af nøje udvalgte kombinationer af metaller, det er muligt at etse indviklede mønstre på en siliciumoverflade, som vist ovenfor. Kredit:Ref. 1 og licenseret under CC BY 4.0 © 2016 L. Kong et -
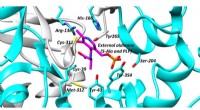 Forskere udforsker racemaser og foreslår strategier til at finde lægemidler, der er målrettet mod…Det aktive sted for alanin racemase, et vigtigt antibakterielt mål. Kredit:University of Bath Forskere fra Storbritanniens University of Bath udforsker racemaser-en vigtig type enzym, der er knytt
Forskere udforsker racemaser og foreslår strategier til at finde lægemidler, der er målrettet mod…Det aktive sted for alanin racemase, et vigtigt antibakterielt mål. Kredit:University of Bath Forskere fra Storbritanniens University of Bath udforsker racemaser-en vigtig type enzym, der er knytt
- Hvad har Hubble -teleskopet bidraget til vores viden om astronomi?
- Hvordan laver man arbejdsmodel af måneformørkelse?
- Hvad kaldes det kontinuerlige ladningsflow?
- Hvilke tilpasninger har planter og dyr i saltvandsbiomer?
- Hvorfor er det vigtigt at have astronuats?
- Graphene 2.0:En ny tilgang til at lave et unikt materiale


