Hvad er nogle kemiske ligninger til oxidation af natriumacetat?
Her er dog nogle mulige scenarier, hvor oxidation kan forekomme sammen med de tilsvarende kemiske ligninger:
1. Forbrænding (oxidation af høj temperatur)
* Ligning:
2 Ch₃coona + 7 O₂ → 4 CO₂ + 4 H₂O + NA₂O
Dette repræsenterer den komplette forbrænding af natriumacetat, der producerer kuldioxid, vand og natriumoxid. Denne reaktion kræver høje temperaturer og en tilstrækkelig forsyning af ilt.
2. Elektrolyse (oxidation ved anoden)
* Ligning:
2 ch₃coo⁻ → 2 co₂ + 2 h₂ + 2e⁻
Denne ligning repræsenterer oxidation af acetationer ved anoden under elektrolyse. Acetationerne mister elektroner og omdannes til kuldioxid og brintgas. Natriumionerne forbliver i opløsning.
3. Reaktion med stærke oxidationsmidler
* Ligning (med kaliumpermanganat):
5 ch₃coona + 8 kmno₄ + 12 h₂so₄ → 10 co₂ + 8 mnso₄ + 4 k₂so₄ + 12 h₂o + 5 na₂so₄
Denne reaktion bruger et stærkt oxidationsmiddel, kaliumpermanganat (KMNO₄), under sure forhold (H₂so₄). Acetationerne oxideres til kuldioxid, mens permanganationerne reduceres.
Vigtige noter:
* specifikke betingelser: De faktiske produkter og reaktioner afhænger stærkt af de specifikke betingelser (temperatur, tryk, tilstedeværelse af katalysatorer osv.).
* Andre reaktioner: Natriumacetat kan også deltage i andre reaktioner, som dekarboxylering (miste en carboxylgruppe) eller hydrolyse (reagerer med vand) uden at blive direkte oxideret.
Det er vigtigt at huske, at oxidation af natriumacetat ikke er en enkel eller ligetil proces. Det kræver specifikke betingelser og involverer ofte tilstedeværelsen af stærke oxidationsmidler eller høje temperaturer.
Sidste artikelHvad er en brintkerner?
Næste artikelHvad er metallisk malm og ikke -malm?
 Varme artikler
Varme artikler
-
 Optisk keramik møder metal-organiske rammerFor nylig, forskere fra Sun Yat-Sen University rapporterede, at ved blot at sænke opløsningsmidlets fordampningshastighed, metalorganiske nanokrystaller kan smelte sammen ved stuetemperatur for at dan
Optisk keramik møder metal-organiske rammerFor nylig, forskere fra Sun Yat-Sen University rapporterede, at ved blot at sænke opløsningsmidlets fordampningshastighed, metalorganiske nanokrystaller kan smelte sammen ved stuetemperatur for at dan -
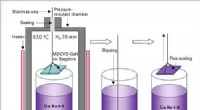 Udvikling af en ny teknik til dyrkning af højkvalitets galliumnitridkrystallerFigur 1. Skematisk af GaN-krystalvækstteknikken ved anvendelse af Flux-Film-Coated Liquid Phase Epitaxy (FFC-LPE) teknikken. Kredit:National Institute for Materials Science Galliumnitridkrystaller
Udvikling af en ny teknik til dyrkning af højkvalitets galliumnitridkrystallerFigur 1. Skematisk af GaN-krystalvækstteknikken ved anvendelse af Flux-Film-Coated Liquid Phase Epitaxy (FFC-LPE) teknikken. Kredit:National Institute for Materials Science Galliumnitridkrystaller -
 Elektrokemisk syntese af formiat fra kuldioxid ved anvendelse af en tin/reduceret grafenoxidkatalysa…Scanning elektronmikroskop billede (øverst til venstre), transmissionselektronmikroskopbillede (øverst til højre), reduktionskarakteristika (nederst til venstre) og Faradic -effektivitet (nederst til
Elektrokemisk syntese af formiat fra kuldioxid ved anvendelse af en tin/reduceret grafenoxidkatalysa…Scanning elektronmikroskop billede (øverst til venstre), transmissionselektronmikroskopbillede (øverst til højre), reduktionskarakteristika (nederst til venstre) og Faradic -effektivitet (nederst til -
 Kemikere udvikler en ny teknologi til at forhindre lithium-ion-batterier i at antændeGasserne byggede sig op og fik det ikke-beskyttede batteri (til venstre) til at svulme op. Det kan føre til en eksplosion. Det beskyttede batteri (til højre) forbliver fladt, da det beskyttende lag bl
Kemikere udvikler en ny teknologi til at forhindre lithium-ion-batterier i at antændeGasserne byggede sig op og fik det ikke-beskyttede batteri (til venstre) til at svulme op. Det kan føre til en eksplosion. Det beskyttede batteri (til højre) forbliver fladt, da det beskyttende lag bl


