Hvorfor er nogle faste stoffer mere tæt end andre faste stoffer?
1. Atommasse:
* tungere atomer: Faststoffer sammensat af tungere atomer har en højere densitet, fordi deres atomer har mere masse pakket i samme volumen. For eksempel er bly tættere end aluminium, fordi blyatomer er meget tungere end aluminiumatomer.
2. Atompakning:
* tæt pakket atomer: Vejatomerne er arrangeret i et fast stof påvirker også densitet. Faststoffer med tæt pakket atomer har en højere densitet, fordi der er mindre tomt mellemrum mellem dem.
* Krystallinske faste stoffer: Disse har en meget ordnet, gentagne struktur, hvilket fører til effektiv pakning.
* amorfe faste stoffer: Disse har en mere tilfældig, mindre organiseret struktur, hvilket ofte resulterer i mindre effektiv pakning.
Her er en analogi:
Forestil dig, at du har to kasser med samme størrelse. Den ene kasse er fyldt med kugler, og den anden er fyldt med ping pong -kugler. Boksen fyldt med kugler vil være tættere, fordi klældene er tungere og mere pakket end ping -pongkuglerne.
Andre faktorer, der kan påvirke densitet:
* Temperatur: Densitet falder typisk med stigende temperatur, fordi atomerne flytter længere fra hinanden.
* tryk: Øget tryk kan komprimere atomerne tættere sammen, hvilket øger densiteten.
* tilstedeværelse af hulrum eller urenheder: Disse kan reducere densitet.
Eksempler:
* jern er tættere end træ Fordi jernatomer er tungere end de atomer, der udgør træ.
* diamant er tættere end grafit Fordi carbonatomer er arrangeret i en tættere pakket struktur i diamant.
Kortfattet: Tætheden af et fast stof bestemmes af massen af dets atomer, og hvor tæt disse atomer pakkes sammen.
Sidste artikelEr zink en god ledervarme og elektricitet?
Næste artikelHvem udviklede moderne atomteori?
 Varme artikler
Varme artikler
-
 Et supermateriale, der kan anvendes til batterier og andre energikonverteringsenhederFirelags atomstruktur af α-KAg 3 Se 2 , en 2D superionisk leder. Atomernes farver er koordineret med farverne i navnet. Kredit:Mercouri Kanatzidis/Northwestern University og Argonne National Labor
Et supermateriale, der kan anvendes til batterier og andre energikonverteringsenhederFirelags atomstruktur af α-KAg 3 Se 2 , en 2D superionisk leder. Atomernes farver er koordineret med farverne i navnet. Kredit:Mercouri Kanatzidis/Northwestern University og Argonne National Labor -
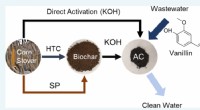 Renere vand gennem majsEn illustration, der viser, hvordan majsstove bliver til biochar, derefter til aktivt kul til vandfiltrering. (Abdul-Aziz et al., 2021) Majs er Amerikas største landbrugsafgrøde, og også en af d
Renere vand gennem majsEn illustration, der viser, hvordan majsstove bliver til biochar, derefter til aktivt kul til vandfiltrering. (Abdul-Aziz et al., 2021) Majs er Amerikas største landbrugsafgrøde, og også en af d -
 Planter kan modstå klimaforandringer og komme sig efter tørke ved at justere lignin-kemiske kodePlanterørscelle forstærket med lignin er meget modstandsdygtig over for undertryk i modsætning til de andre fladtrykte celler omkring. Kredit:Cheng Choo Lee En ny undersøgelse viser, at vi kan skab
Planter kan modstå klimaforandringer og komme sig efter tørke ved at justere lignin-kemiske kodePlanterørscelle forstærket med lignin er meget modstandsdygtig over for undertryk i modsætning til de andre fladtrykte celler omkring. Kredit:Cheng Choo Lee En ny undersøgelse viser, at vi kan skab -
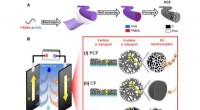 Porøse kulstof nanofibre demonstrerer exceptionel kapacitiv deioniseringSkematiske illustrationer af PCF-forberedelse og kapacitiv deionisering. (A) Syntese af PCF fra PMMA-b-PAN via elektrospinning af PMMA-b-PAN til fibre, selvsamling af PMMA-b-PAN til uordnede, bikontin
Porøse kulstof nanofibre demonstrerer exceptionel kapacitiv deioniseringSkematiske illustrationer af PCF-forberedelse og kapacitiv deionisering. (A) Syntese af PCF fra PMMA-b-PAN via elektrospinning af PMMA-b-PAN til fibre, selvsamling af PMMA-b-PAN til uordnede, bikontin
- Hvad er den relative placering af Ecuador?
- Områder langs en fejl, hvor der er sket relativitet få jordskælv?
- Jordskælvfrigivelsesenergi i form af?
- Hvad opbevarer batterier?
- Hvad er formlen for en forbindelse fra SR og BR?
- Hvorfor bruger du enzym tomt og underlag i stedet for en enkelt for at finde ud af aktiviteten?


