Hvorfor flyder væsker let, mens faste stoffer ikke er?
væsker:
* Partikler er tæt sammen, men kan bevæge sig rundt: I modsætning til faste stoffer, hvor partikler er tæt pakket og fastgjort i position, har flydende partikler mere frihed til at bevæge sig. De er stadig tæt nok til at udøve attraktive kræfter på hinanden, men disse kræfter er svagere end i faste stoffer.
* Fluid Natur: Denne bevægelsesfrihed giver flydende partikler mulighed for let at glide forbi hinanden, hvilket giver væsker deres karakteristiske fluiditet. De kan tage formen på deres beholder, fordi deres partikler kan strømme for at fylde den tilgængelige plads.
* Viskositet: Væsker har en vis modstand mod flow, der kaldes viskositet. Dette skyldes de attraktive kræfter mellem partikler, der lidt modstår deres bevægelse. Tykkere væsker har højere viskositet end tyndere væsker.
faste stoffer:
* Partikler er tæt pakket og faste i position: Faste partikler holdes i en stiv, ordnet struktur af stærke attraktive kræfter. De vibrerer på plads, men bevæger sig ikke frit rundt.
* bestemt form: På grund af det faste arrangement af partikler har faste stoffer en bestemt form og volumen. De modstår ethvert forsøg på at ændre deres form, hvilket får dem til at virke stive.
* krystallinsk vs. amorf: Faststoffer kan være krystallinsk, hvor partikler er arrangeret i et regelmæssigt, gentagende mønster (som salt) eller amorf, hvor partikler er arrangeret tilfældigt (som glas).
Kortfattet:
Væsker flyder let, fordi deres partikler kan bevæge sig forbi hinanden på grund af svagere attraktive kræfter og mere bevægelsesfrihed. På den anden side er faste stoffer stive, fordi deres partikler er fastgjort i position af stærke attraktive kræfter.
Sidste artikelHvilken tilstand af stof har de hurtigste molekyler?
Næste artikelHvad er funktionen af grafit i en atomreaktor?
 Varme artikler
Varme artikler
-
 Værktøjssæt:Brug af lokal jord til 3D-print af store strukturer(A) Illustration af geopolymerisationstilgang udviklet til at størkne moskus til en bærende silikatkomposit, som repræsenteret ved kraften af et bildæk på vej forstærket af kompositmaterialet, genop
Værktøjssæt:Brug af lokal jord til 3D-print af store strukturer(A) Illustration af geopolymerisationstilgang udviklet til at størkne moskus til en bærende silikatkomposit, som repræsenteret ved kraften af et bildæk på vej forstærket af kompositmaterialet, genop -
 Nanofiltreringsmembraner til behandling af industrielt spildevand fra tungmetallerKredit:National University of Science and Technology MISIS NUST MISIS -forskere præsenterede sammen med indiske kolleger fra Jain University og Sri Dharmasthala Manjunatheshwara College innovative
Nanofiltreringsmembraner til behandling af industrielt spildevand fra tungmetallerKredit:National University of Science and Technology MISIS NUST MISIS -forskere præsenterede sammen med indiske kolleger fra Jain University og Sri Dharmasthala Manjunatheshwara College innovative -
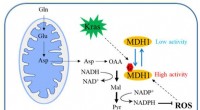 Forskere identificerer O-GlcNAcylering som årsag til bugspytkirteltumorvækst ved at regulere MDH1Skematisk diagram af, hvordan MDH1-glykosylering regulerer PDAC-vækst. Kredit:Zhejiang University Bugspytkirtelkræft er en yderst ondartet tumor i fordøjelsessystemet, og dens femårige overlevelses
Forskere identificerer O-GlcNAcylering som årsag til bugspytkirteltumorvækst ved at regulere MDH1Skematisk diagram af, hvordan MDH1-glykosylering regulerer PDAC-vækst. Kredit:Zhejiang University Bugspytkirtelkræft er en yderst ondartet tumor i fordøjelsessystemet, og dens femårige overlevelses -
 Mediciner 3D-printet på syv sekunderKredit:University College London Medicin kan printes på syv sekunder i en ny 3D-printteknik, der kan muliggøre hurtig on-site produktion af medicin, rapporterer et UCL-ledet forskerhold. Resultate
Mediciner 3D-printet på syv sekunderKredit:University College London Medicin kan printes på syv sekunder i en ny 3D-printteknik, der kan muliggøre hurtig on-site produktion af medicin, rapporterer et UCL-ledet forskerhold. Resultate
- Hvorfor er valenselektronerne i metalliske bindinger forskellige fra andre på grund af hvad?
- Bliver økologisk frugt, grøntsager snart billigere?
- Hvor findes jernoxid?
- Rækker økologien helt ned til den subatomære skala?
- Økolim kan erstatte skadelige klæbemidler i træbyggeri
- Edgy kig på 2-D molybdendisulfid


