Hvorfor er voks sværere at antænde end metan?
1. Kemisk sammensætning:
* methan (CH4): Metan er et simpelt carbonhydrid med et enkelt carbonatom og fire hydrogenatomer. Det er meget brandfarligt, fordi det let reagerer med ilt i luften.
* voks: Voks er en kompleks blanding af kulbrinter med lange kæder af carbonatomer og brintatomer. Disse kæder er mere stabile og mindre reaktive end den enkle struktur af metan.
2. Volatilitet:
* methan: Metan er en gas ved stuetemperatur og har et lavt kogepunkt. Dette betyder, at det let fordamper og blandes med luft og skaber en brandfarlig blanding.
* voks: Voks er et fast stof ved stuetemperatur og har et højt smeltepunkt. Det kræver betydelig varme for at fordampe og skabe en brandfarlig blanding.
3. Overfladeareal:
* methan: Metan er en gas, så den har et stort overfladeareal, der let interagerer med ilt.
* voks: Voks er et fast stof, så det har et mindre overfladeareal, der reducerer reaktionshastigheden med ilt.
4. Tændingstemperatur:
* methan: Metan har en relativt lav antændelsestemperatur, hvilket betyder, at den kan antænde ved en lavere temperatur sammenlignet med voks.
* voks: Voks har en højere antændelsestemperatur, der kræver mere varme for at begynde at brænde.
5. Energiindhold:
* methan: Metan er et meget energisk brændstof, hvilket betyder, at den frigiver en stor mængde energi, når den brændes.
* voks: Mens voks også har energiindhold, er det mindre energisk end metan pr. Enhedsmasse.
Kortfattet:
Den komplekse struktur, lav volatilitet, mindre overfladeareal, højere antændelsestemperatur og lavere energiindhold i voks gør det vanskeligere at antænde sammenlignet med metan.
 Varme artikler
Varme artikler
-
 Sporing af bortskaffelse af proteiner kan føre til forbedrede behandlingerHiroaki Kiyokawa, MD, Ph.d., professor i farmakologi og patologi, var co-senior forfatter på undersøgelser publiceret i Naturkommunikation og Videnskabens fremskridt . Kredit:Northwestern Universi
Sporing af bortskaffelse af proteiner kan føre til forbedrede behandlingerHiroaki Kiyokawa, MD, Ph.d., professor i farmakologi og patologi, var co-senior forfatter på undersøgelser publiceret i Naturkommunikation og Videnskabens fremskridt . Kredit:Northwestern Universi -
 Åbner den sorte boks af heterogen katalyseKredit:Institut for Kemisk Forskning i Catalonien Forskere fra ICIQs López-gruppe præsenterer en ny metode, der giver mulighed for rationelt design af heterogene katalysatorer. Efter anvendelse af
Åbner den sorte boks af heterogen katalyseKredit:Institut for Kemisk Forskning i Catalonien Forskere fra ICIQs López-gruppe præsenterer en ny metode, der giver mulighed for rationelt design af heterogene katalysatorer. Efter anvendelse af -
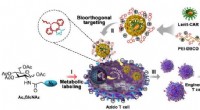 Forskere udvikler kunstige kemiske receptorer til at hjælpe viral transduktion til T-celleteknikAnvendelse af kunstig kemisk receptor i CAR-konstrueret T-cellefremstilling og immunterapi af tumor. Kredit:CAI Lintao Konstrueret T-celle immunterapi, såsom kimærisk antigenreceptor T-celle (CAR-
Forskere udvikler kunstige kemiske receptorer til at hjælpe viral transduktion til T-celleteknikAnvendelse af kunstig kemisk receptor i CAR-konstrueret T-cellefremstilling og immunterapi af tumor. Kredit:CAI Lintao Konstrueret T-celle immunterapi, såsom kimærisk antigenreceptor T-celle (CAR- -
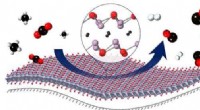 Katalysator for bæredygtig gassynteseEn tynd film af metaloxycarbider på en oxidbærer letter reaktionen mellem CO 2 og methan (CH4) til fremstilling af hydrogen (H2) og kulilte (CO). Kredit:Alexey Kurlov, Evgenia Deeva / ETH Zürich
Katalysator for bæredygtig gassynteseEn tynd film af metaloxycarbider på en oxidbærer letter reaktionen mellem CO 2 og methan (CH4) til fremstilling af hydrogen (H2) og kulilte (CO). Kredit:Alexey Kurlov, Evgenia Deeva / ETH Zürich
- Hvad er en enhed eller materiale, der tillader strøm at strømme let gennem det?
- Nanoteknologisk beskyttelse:Det nuværende sikkerhedsudstyr er muligvis ikke tilstrækkeligt til nan…
- Er Texas tættere på den nordlige eller Sydpol?
- Hvordan oversættes RNA, og hvor?
- Hvorfor er Mars Sky rød?
- Stiger månen senere hver dag på grund af sin revolution mod uret rundt om i jorden?


