Hvilken kraft skal overvindes for at ændre et fast stof til væske?
Her er hvorfor:
* faste stoffer: I et fast stof er partiklerne tæt pakket og holdes sammen af stærke intermolekylære kræfter. Disse kræfter holder partiklerne i en fast, stiv struktur.
* væsker: I en væske har partiklerne større bevægelsesfrihed. Mens de stadig er tiltrukket af hinanden, er de intermolekylære kræfter svagere, hvilket giver partiklerne mulighed for at glide forbi hinanden.
For at smelte et fast stof skal du tilvejebringe nok energi (normalt i form af varme) til at overvinde de intermolekylære kræfter, der holder partiklerne i en stiv struktur. Dette giver dem mulighed for at bevæge sig mere frit og overgang til flydende tilstand.
Styrken af de intermolekylære kræfter bestemmer smeltepunktet for et stof. Stoffer med stærke intermolekylære kræfter har højere smeltepunkter, fordi det tager mere energi at overvinde dem.
Sidste artikelHvad sker der, når 2 atomer er ret tæt på?
Næste artikelHvilke materialer overfører ikke varmen let?
 Varme artikler
Varme artikler
-
 Organisk/uorganisk svovl kan være nøglen til sikre genopladelige lithiumbatterierEt af de lithium svovl møntbatterier, der udvikles i Penn States Energy Nanostructure Laboratory (E-Nano). Kredit:Patrick Mansell, Penn State Vi er kommet langt fra utætte svovlsyre-bilbatterier,
Organisk/uorganisk svovl kan være nøglen til sikre genopladelige lithiumbatterierEt af de lithium svovl møntbatterier, der udvikles i Penn States Energy Nanostructure Laboratory (E-Nano). Kredit:Patrick Mansell, Penn State Vi er kommet langt fra utætte svovlsyre-bilbatterier, -
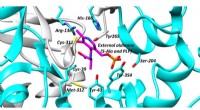 Forskere udforsker racemaser og foreslår strategier til at finde lægemidler, der er målrettet mod…Det aktive sted for alanin racemase, et vigtigt antibakterielt mål. Kredit:University of Bath Forskere fra Storbritanniens University of Bath udforsker racemaser-en vigtig type enzym, der er knytt
Forskere udforsker racemaser og foreslår strategier til at finde lægemidler, der er målrettet mod…Det aktive sted for alanin racemase, et vigtigt antibakterielt mål. Kredit:University of Bath Forskere fra Storbritanniens University of Bath udforsker racemaser-en vigtig type enzym, der er knytt -
 Brug af koffein som katalysator, forskere skaber nye geler til medicinafgivelseForskere fra MIT og Brigham og Womens Hospital har udtænkt en ny måde at skabe fleksible polymergeler ved hjælp af koffein som katalysator. Kredit:Massachusetts Institute of Technology Koffein er
Brug af koffein som katalysator, forskere skaber nye geler til medicinafgivelseForskere fra MIT og Brigham og Womens Hospital har udtænkt en ny måde at skabe fleksible polymergeler ved hjælp af koffein som katalysator. Kredit:Massachusetts Institute of Technology Koffein er -
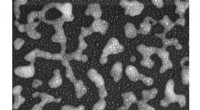 Kemisk sensing-chip opsnuser kokain inden for få minutterEt scanningselektronmikroskopbillede viser overfladen af en ny kemisk sensing-chip. Overfladen består af guld nanopartikler (små lyse prikker), der er blevet aflejret over sølv nanopartikler (lysegr
Kemisk sensing-chip opsnuser kokain inden for få minutterEt scanningselektronmikroskopbillede viser overfladen af en ny kemisk sensing-chip. Overfladen består af guld nanopartikler (små lyse prikker), der er blevet aflejret over sølv nanopartikler (lysegr
- Er Mars kendt for romerske guder?
- Hvad sker der med partiklernes hastigheder, når termisk ledning forekommer inden for et fast stof?
- Politisk polarisering? Giv ikke nettet skylden, siger undersøgelse
- Ville mikroøkologi blive beskadiget af en plastikfilm, der dræber skadelige jordinsekter?
- Selvflyvende svævefly lærer at svæve som en fugl
- Handelskrig mellem USA og Kina bringer Amazonaskoven i fare, eksperter advarer


