I partikelteori Hvorfor går flydende til fast?
1. Partikeladfærd i væsker:
- Partikler i en væske har moderat kinetisk energi, så de kan bevæge sig frit, men de er stadig tæt på hinanden.
- De har et bestemt volumen, men tager formen på deres beholder.
2. Partikeladfærd i faste stoffer:
- Partikler i et fast stof har signifikant lavere kinetisk energi sammenlignet med væsker.
- Denne lavere energi får partiklerne til at vibrere i faste positioner og danner en stiv struktur.
- Faststoffer har et bestemt volumen og form.
3. Overgangen:
- Når du afkøler en væske, mister partiklerne kinetisk energi.
- Denne reduktion i energi får partiklerne til at bremse og bevæge sig tættere sammen.
- Til sidst bliver de attraktive kræfter mellem partiklerne stærke nok til at overvinde deres bevægelse, hvilket får dem til at låse i et fast arrangement og danne et solidt.
Kortfattet: Overgangen fra væske til fast er grundlæggende om, at partiklerne mister energi og bliver mere tæt pakket, hvilket fører til en stiv struktur.
Her er nogle yderligere faktorer, der kan påvirke denne overgang:
- tryk: Stigende tryk kan også tvinge partikler tættere sammen og fremme størkning.
- Type stof: Forskellige stoffer har forskellige styrker af intermolekylære kræfter, som påvirker temperaturen, hvormed de størkner.
- Krystallinsk vs. amorfe faste stoffer: Strukturen af det faste stof kan være enten krystallinsk (meget ordnet) eller amorf (forstyrret).
Fortæl mig, hvis du gerne vil have flere detaljer om et specifikt aspekt af denne proces!
Sidste artikelHvad er ikke subatomære partikler?
Næste artikelHvordan bevæger molekyler sig i en væske?
 Varme artikler
Varme artikler
-
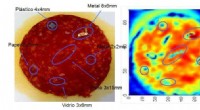 Design af sensorer til at detektere fremmedlegemer i fødevarerBillede opnået med denne teknologi, hvor der kan ses, på et stykke pølse, plast, metaller og splinter af glas i forskellige størrelser og former. Kredit:Elhuyar Fundazioa Forskere ved NUP/UPNA-Pub
Design af sensorer til at detektere fremmedlegemer i fødevarerBillede opnået med denne teknologi, hvor der kan ses, på et stykke pølse, plast, metaller og splinter af glas i forskellige størrelser og former. Kredit:Elhuyar Fundazioa Forskere ved NUP/UPNA-Pub -
 Forskere rapporterer om cellegennemtrængelige nanobodiesRingpeptider åbner cellemembrandøren og tillader antistoffer og andre terapeutiske midler at trænge ind i cellerne. Kredit:Christoph Hohmann, Nanosystems Initiative München (NIM) Forskere ved Tech
Forskere rapporterer om cellegennemtrængelige nanobodiesRingpeptider åbner cellemembrandøren og tillader antistoffer og andre terapeutiske midler at trænge ind i cellerne. Kredit:Christoph Hohmann, Nanosystems Initiative München (NIM) Forskere ved Tech -
 Kemikere opnår gennembrud i produktionen af tredimensionelle molekylære strukturerKemikere bruger denne eksperimentelle opsætning til fotokemiske reaktioner. Kredit:Peter Bellotti Et vigtigt mål for organisk og medicinsk kemi i de seneste årtier har været den hurtige syntese af
Kemikere opnår gennembrud i produktionen af tredimensionelle molekylære strukturerKemikere bruger denne eksperimentelle opsætning til fotokemiske reaktioner. Kredit:Peter Bellotti Et vigtigt mål for organisk og medicinsk kemi i de seneste årtier har været den hurtige syntese af -
 Forskere udstyrer kemiske sensorer med fælder til at opdage giftige stofferAss. Prof. Pavel Postnikov i laboratoriet. Kredit:Tomsk Polytekniske Universitet Forskere fra Tomsk Polytechnic University og University of Chemistry and Technology (Prag, Tjekkiet) har skabt nye
Forskere udstyrer kemiske sensorer med fælder til at opdage giftige stofferAss. Prof. Pavel Postnikov i laboratoriet. Kredit:Tomsk Polytekniske Universitet Forskere fra Tomsk Polytechnic University og University of Chemistry and Technology (Prag, Tjekkiet) har skabt nye


