Hvad er gassen af hotness eller kulde?
Her er hvorfor:
* Temperatur: Hotness og kulde er relateret til temperatur. Temperaturen er et mål for den gennemsnitlige kinetiske energi for partiklerne i et stof.
* kinetisk energi: Kinetisk energi er bevægelsesenergien. Når partikler bevæger sig hurtigere, har de højere kinetisk energi, og stoffet føles varmere. Når partikler bevæger sig langsommere, har de lavere kinetisk energi, og stoffet føles koldere.
Gasser, væsker og faste stoffer: Materialet (gas, væske eller faste) påvirker, hvor let partiklerne kan bevæge sig.
* Gasser: Gaspartikler har den højeste kinetiske energi og bevæger sig frit.
* væsker: Flydende partikler har mindre kinetisk energi end gasser og kan bevæge sig rundt i hinanden.
* faste stoffer: Faste partikler har den laveste kinetiske energi og er tæt pakket sammen og vibrerer på plads.
Sammendrag: Hotness og kulde er ikke stoffer. De er egenskaber ved stof, der afspejler partiklernes gennemsnitlige kinetiske energi inden for den sag.
Sidste artikelNår molekyler af luft skubbes sammen, danner de et højt højt tryk, der kaldes A?
Næste artikelHvor mange gasenheder i 47 kg?
 Varme artikler
Varme artikler
-
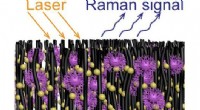 En hurtig og billig enhed til at fange og identificere viraArray af nanorør dekoreret med guld nanopartikler fanger virusmolekyler. Kredit:Terrones Lab/Penn State En enhed til hurtigt at fange og identificere forskellige virusstammer er blevet udviklet, i
En hurtig og billig enhed til at fange og identificere viraArray af nanorør dekoreret med guld nanopartikler fanger virusmolekyler. Kredit:Terrones Lab/Penn State En enhed til hurtigt at fange og identificere forskellige virusstammer er blevet udviklet, i -
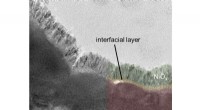 Solbrint:Fotoanoder lover høj effektivitetTEM-billede af en α-SnWO4 film (grøn) overtrukket med 20 nm NiOx (pink). Ved grænsefladen mellem α-SnWO4 og NiOx kan et yderligere grænsefladelag observeres. Kredit:HZB Fotoanoder fremstillet af m
Solbrint:Fotoanoder lover høj effektivitetTEM-billede af en α-SnWO4 film (grøn) overtrukket med 20 nm NiOx (pink). Ved grænsefladen mellem α-SnWO4 og NiOx kan et yderligere grænsefladelag observeres. Kredit:HZB Fotoanoder fremstillet af m -
 Forskere foreslår, at man anvender metanoverflader af guld til at bestemme stoffets molekylære sam…Guldpartikler Kredit:Dmitry Bayer En ny metode vil gøre det muligt at skabe kompakte enheder, der nøjagtigt bestemmer den molekylære sammensætning af en væske eller gas, og hjælpe med at identific
Forskere foreslår, at man anvender metanoverflader af guld til at bestemme stoffets molekylære sam…Guldpartikler Kredit:Dmitry Bayer En ny metode vil gøre det muligt at skabe kompakte enheder, der nøjagtigt bestemmer den molekylære sammensætning af en væske eller gas, og hjælpe med at identific -
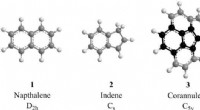 Interstellar kemi:lavtemperaturgasfasedannelse af inden i det interstellare mediumDe enkleste repræsentanter for to-ring PAHer, der bærer to seks-leddede (naphthalen, C10H8; 1) og en seks- sammen med en fem-leddet ring (indene, C9H8; 2). Mens hydrogenabstraktion-vinylacetylen-addit
Interstellar kemi:lavtemperaturgasfasedannelse af inden i det interstellare mediumDe enkleste repræsentanter for to-ring PAHer, der bærer to seks-leddede (naphthalen, C10H8; 1) og en seks- sammen med en fem-leddet ring (indene, C9H8; 2). Mens hydrogenabstraktion-vinylacetylen-addit
- Hvilken planet har en lignende længde på dagen som Jorden?
- Nissan ændrer ikke autonome køreprøver over Uber -styrt
- Ingeniører opnår verdensrekord med højhastighedsgrafen-transistorer
- Et andet ord for stat i videnskab?
- Udtynding af ozonlaget kan have drevet Jordens største masseudryddelse for 252 millioner år siden
- Hvorfor ser vi solen et kort øjeblik, efter at den er indstillet?


