Temperaturen, hvormed en væskes damptryk er lig med ekstern, hvad?
Her er hvorfor:
* damptryk: Hver væske har en tendens til at fordampe, og dens molekyler slipper ud i gasfasen. Denne undslipende tendens skaber et tryk kaldet damptryk. Jo højere temperatur, jo flere molekyler har nok energi til at flygte, og jo højere damptryk.
* eksternt tryk: Dette er det tryk, der udøves af den omgivende atmosfære på væskens overflade.
* kogepunkt: Når væskens damptryk er lig med det ydre tryk, begynder væsken at koge. Dette skyldes, at de flugtende molekyler har nok energi til at overvinde trykket, der skubber ned på væskens overflade.
Fortæl mig, hvis du gerne vil vide mere om damptryk eller kogepunkt!
 Varme artikler
Varme artikler
-
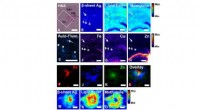 Kombineret billeddannelsestilgang karakteriserer plaques forbundet med Alzheimers sygdomHistologi, FTIR, XFM, og vævsautofluorescensbilleddannelse af Aβ-plaques. Kredit:University of Adelaide Australske synkrotron røntgen og infrarød billeddannelsesteknikker er blevet brugt i en kraf
Kombineret billeddannelsestilgang karakteriserer plaques forbundet med Alzheimers sygdomHistologi, FTIR, XFM, og vævsautofluorescensbilleddannelse af Aβ-plaques. Kredit:University of Adelaide Australske synkrotron røntgen og infrarød billeddannelsesteknikker er blevet brugt i en kraf -
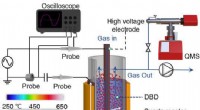 Ikke-termisk plasma-promoveret CO2-hydrogenering i nærværelse af legeringskatalysatorerFigur 1. Kuldioxidgenanvendelse - innovativt plasmakatalysekoncept. Dielektrisk barriereudladningsreaktor med fluidiseret leje blev brugt til CO2-hydrogenering over Pd2 Ga/SiO2 . Kredit:Journal of the
Ikke-termisk plasma-promoveret CO2-hydrogenering i nærværelse af legeringskatalysatorerFigur 1. Kuldioxidgenanvendelse - innovativt plasmakatalysekoncept. Dielektrisk barriereudladningsreaktor med fluidiseret leje blev brugt til CO2-hydrogenering over Pd2 Ga/SiO2 . Kredit:Journal of the -
 Inspireret af kombucha te, ingeniører skaber levende materialerKredit:Imperial College London Ingeniører på MIT og Imperial College London har udviklet en ny måde at generere hårde, funktionelle materialer ved hjælp af en blanding af bakterier og gær, der lig
Inspireret af kombucha te, ingeniører skaber levende materialerKredit:Imperial College London Ingeniører på MIT og Imperial College London har udviklet en ny måde at generere hårde, funktionelle materialer ved hjælp af en blanding af bakterier og gær, der lig -
 Et intelligent blødt materiale, der krøller under tryk eller udvider sig, når det strækkesEt intelligent blødt materiale kan krølle under tryk eller mekanisk belastning. Kredit:American Chemical Society Planter og dyr kan hurtigt reagere på ændringer i deres miljø, såsom en Venus flyve
Et intelligent blødt materiale, der krøller under tryk eller udvider sig, når det strækkesEt intelligent blødt materiale kan krølle under tryk eller mekanisk belastning. Kredit:American Chemical Society Planter og dyr kan hurtigt reagere på ændringer i deres miljø, såsom en Venus flyve
- Hvad er forbindelsen mellem hastighed og acceleration?
- Disse organismer arbejder sammen for at genbruge materialer gennem et økosystem?
- Sådan huskes afgifterne for polyatomiske joner <p> <p> Ioner i kemi kan være et enkelt ladet atom,…
- Hvilken tilstand af materie er magma?
- Australien markerer skrappe nye databeskyttelseslove i år
- Molekylært tynd hybrid perovskit til avancerede optoelektroniske applikationer


