Hvad menes med de Broglie -bølgelængden af en partikel?
Nøglekoncepter:
* bølgepartikel dualitet: De Broglies hypotese udvidede bølgepartikeldualitetskonceptet (allerede etableret for lys) til at gøre noget. Han foreslog, at alle stof udviser bølglignende egenskaber.
* momentum: Momentumet for en partikel er et mål for dens masse og hastighed. Det er en vektormængde (med både størrelse og retning).
* bølgelængde: Bølgelængde er afstanden mellem to på hinanden følgende kamre eller trug af en bølge.
Formel:
De Broglie -bølgelængden (λ) af en partikel er givet af:
`` `
λ =h / p
`` `
hvor:
* λ er de broglie bølgelængde
* h er Plancks konstante (6.626 x 10⁻³⁴ J · s)
* p er momentumet for partiklen (masse * hastighed)
Betydning:
De Broglie -bølgelængden hjælper os med at forstå:
* bølgelignende opførsel af stof: Det forklarer, hvorfor partikler som elektroner kan udvise diffraktion og interferensmønstre, ligesom bølger.
* kvante karakter af stof: Det afslører, at partiklernes opførsel på atom- og subatomisk niveau ikke kan forklares med klassisk fysik alene og kræver kvantemekanik.
* applikationer: De Broglies koncept har betydelige applikationer inden for felter som:
* Elektronmikroskopi: Ved hjælp af elektronernes bølgelignende natur til at skabe billeder i høj opløsning.
* kvanteberegning: Brug af bølgeegenskaber for partikler til beregning.
Eksempel:
Overvej et elektron med et momentum på 1,0 x 10⁻²⁴ kg · m/s. Dens de broglie -bølgelængde ville være:
`` `
λ =(6,626 x 10⁻³⁴ j · s) / (1,0 x 10⁻²⁴ kg · m / s) =6,626 x 10⁻¹⁰ m
`` `
Denne bølgelængde falder inden for rækkevidden af røntgenstråler, hvilket indikerer den bølgelignende natur af elektroner ved dette momentum.
Vigtig note: De Broglie -bølgelængden bliver kun signifikant ved meget små skalaer (atom- og subatomiske niveauer). For makroskopiske genstande er bølgelængden ekstremt lille og praktisk talt ikke påviselig.
 Varme artikler
Varme artikler
-
 Fremtiden for biobrændstoffer i mørketLab-dyrkede alger. Kredit:Elizabeth Hann/UCR Alger kunne konkurrere med petroleum som fremtidens brændstof, hvis blot processen med at dyrke det var mere effektiv. Takket være et stipendium fra Li
Fremtiden for biobrændstoffer i mørketLab-dyrkede alger. Kredit:Elizabeth Hann/UCR Alger kunne konkurrere med petroleum som fremtidens brændstof, hvis blot processen med at dyrke det var mere effektiv. Takket være et stipendium fra Li -
 Ny forskning viser, hvordan grupperede partikler bestemmer elasticiteten af nogle gelerEt team af forskere, herunder UDs Eric Furst, opdagede, at gelernes elasticitet stammer fra pakning af klynger af partikler i gelerne, som gruppen kaldte lokalt glasagtige klynger. Kredit:Eric Furst,
Ny forskning viser, hvordan grupperede partikler bestemmer elasticiteten af nogle gelerEt team af forskere, herunder UDs Eric Furst, opdagede, at gelernes elasticitet stammer fra pakning af klynger af partikler i gelerne, som gruppen kaldte lokalt glasagtige klynger. Kredit:Eric Furst, -
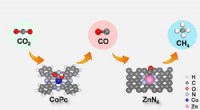 Tandemkatalysator til forbedring af kuldioxidelektroreduktion til metanCO2 reduceres først elektrokemisk til CO og derefter diffunderer CO til Zn-N-C for yderligere omdannelse til CH 4 over CoPc@Zn-N-C tandemkatalysator. Kredit:LIN Long og LIU Tianfu Kuldioxidreduk
Tandemkatalysator til forbedring af kuldioxidelektroreduktion til metanCO2 reduceres først elektrokemisk til CO og derefter diffunderer CO til Zn-N-C for yderligere omdannelse til CH 4 over CoPc@Zn-N-C tandemkatalysator. Kredit:LIN Long og LIU Tianfu Kuldioxidreduk -
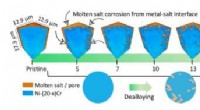 Forskere ser smeltede salte skære små kroge og tunneler ind i metallegeringer i 3DIllustrationen viser, hvordan smeltet salt over tid fjerner metallisk materiale (blå) fra prøven i 3D (øvre) og 2D -visualiseringer (nedre). Denne proces, såkaldt dealloying skaber et bikontinuerligt
Forskere ser smeltede salte skære små kroge og tunneler ind i metallegeringer i 3DIllustrationen viser, hvordan smeltet salt over tid fjerner metallisk materiale (blå) fra prøven i 3D (øvre) og 2D -visualiseringer (nedre). Denne proces, såkaldt dealloying skaber et bikontinuerligt
- Hvilken type fejl er forbundet med filateliske bjerge?
- Human Interaction With Coral Reefs
- SuperTIGER ballon flyver igen for at studere tunge kosmiske partikler
- Hvad er formålet med, at bagepulver og eddike blæser en ballon i luften?
- Hvad er den moderne elektronkonfiguration af svovl?
- Huawei kæmper med USA om spionagefrygt til topmobilmessen


