Hvad er forholdet mellem reaktanter og produkter i en kemisk ligning?
reaktanter:
* Startmaterialer: Dette er de stoffer, der er til stede i begyndelsen af en kemisk reaktion.
* gennemgå transformation: De omdannes til nye stoffer under reaktionen.
* placeret på venstre side: I en kemisk ligning skrives reaktanter typisk på venstre side af pilen.
Produkter:
* resulterende stoffer: Dette er de stoffer, der dannes som et resultat af den kemiske reaktion.
* oprettet af reaktionen: De er skabt af omarrangementet af atomer inden for reaktanterne.
* placeret på højre side: Produkter skrives typisk på højre side af pilen i en kemisk ligning.
forhold:
* Transformation: Reaktanter omdannes til produkter ved at bryde og danne kemiske bindinger.
* bevarelse af masse: Den samlede masse af reaktanterne skal svare til den samlede masse af produkterne. Dette er loven om bevarelse af masse.
* støkiometri: Koefficienterne i en afbalanceret kemisk ligning repræsenterer de relative mængder (mol) af reaktanter og produkter involveret i reaktionen.
Eksempel:
Overvej forbrænding af metan:
CH₄ (G) + 2O₂ (G) → CO₂ (G) + 2H₂O (G)
* reaktanter: Metan (ch₄) og ilt (o₂)
* Produkter: Kuldioxid (co₂) og vand (H₂O)
I denne reaktion reagerer methan og ilt på dannelse af kuldioxid og vand. De kemiske bindinger i reaktanterne er brudt, og nye bindinger dannes i produkterne. Antallet af atomer i hvert element forbliver det samme på begge sider af ligningen, hvilket viser loven om bevarelse af masse.
Nøgle takeaways:
* Reaktanter er udgangsmaterialer for en reaktion, og produkter er de stoffer, der dannes som et resultat.
* Forholdet mellem reaktanter og produkter er en transformation drevet af brud og dannelse af kemiske bindinger.
* Loven om bevarelse af masse styrer forholdet og sikrer, at masse hverken skabes eller ødelægges under en kemisk reaktion.
 Varme artikler
Varme artikler
-
 Ferroelektriske selvsamlede molekylære materialerDet første materiale med konduktivitetsegenskaber, der kan tændes og slukkes ved hjælp af ferroelektrisk polarisering. Kredit:Thor Balkhed Professor Martijn Kemerink fra Linköping Universitet har
Ferroelektriske selvsamlede molekylære materialerDet første materiale med konduktivitetsegenskaber, der kan tændes og slukkes ved hjælp af ferroelektrisk polarisering. Kredit:Thor Balkhed Professor Martijn Kemerink fra Linköping Universitet har -
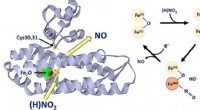 Identifikation af enzym involveret i stresshåndtering hos bakterierGrafisk abstrakt. Kredit:Journal of the American Chemical Society (2022). DOI:10.1021/jacs.1c12407 Forskere fra University of East Anglia har identificeret en ny klasse af enzymer involveret i stre
Identifikation af enzym involveret i stresshåndtering hos bakterierGrafisk abstrakt. Kredit:Journal of the American Chemical Society (2022). DOI:10.1021/jacs.1c12407 Forskere fra University of East Anglia har identificeret en ny klasse af enzymer involveret i stre -
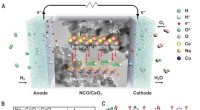 Reduktion af driftstemperaturen for keramiske brændselsceller med en elektrolyt med høj protonledn…Design af NCO/CeO2-heterostrukturfunktionerne til hurtig protonmigrering. Kredit: Videnskab (2020). DOI:10.1126/science.aaz9139 Et team af forskere tilknyttet flere institutioner i Kina har udvik
Reduktion af driftstemperaturen for keramiske brændselsceller med en elektrolyt med høj protonledn…Design af NCO/CeO2-heterostrukturfunktionerne til hurtig protonmigrering. Kredit: Videnskab (2020). DOI:10.1126/science.aaz9139 Et team af forskere tilknyttet flere institutioner i Kina har udvik -
 Selvvandende jord kan ændre landbrugetForskere plantede radiser i dette miniaturedrivhus ved hjælp af deres selvvandende jord og sammenlignede det med sandjord, der findes i tørre områder af verden. Kredit:University of Texas i Austin
Selvvandende jord kan ændre landbrugetForskere plantede radiser i dette miniaturedrivhus ved hjælp af deres selvvandende jord og sammenlignede det med sandjord, der findes i tørre områder af verden. Kredit:University of Texas i Austin
- Hvordan solvarme driver hurtig smeltning af dele af Antarktis største ishylde
- Design og genanvendelse af celleceptorer
- En mere sikker måde at implementere bakterier som miljøsensorer
- Et objekt, der har den samme hastighed, men ændrer retning er?
- Hvor mange orkaner er på Mars?
- Everest bjergbestigere bogstaver digitaliseret for første gang


