Hvilken første ioniseringsenergi er den mest sandsynlige for et meget reaktivt metal?
* ioniseringsenergi: Dette er den energi, der kræves for at fjerne et elektron fra et neutralt atom i dens gasformige tilstand.
* reaktivitet: Metaller er reaktive, fordi de let mister elektroner til at danne positive ioner (kationer). Dette gør dem til gode reduktionsmidler.
* forhold: Jo lettere det er at fjerne en elektron (lavere ioniseringsenergi), jo lettere vil metallet danne en kation og deltage i kemiske reaktioner.
Eksempel:
* Alkalimetaller (som lithium, natrium, kalium) er ekstremt reaktive. De har meget lave første ioniseringsenergier, fordi deres yderste elektron er relativt løst holdt.
Derfor ville et meget reaktivt metal sandsynligvis have en første ioniseringsenergi i området 5-10 elektronvolt (EV).
Sidste artikelHvad er tre forskellige slags termomenter?
Næste artikelHvad er termisk ekspansion i gasser?
 Varme artikler
Varme artikler
-
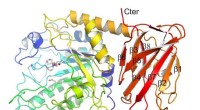 Forskere analyserer 3-D-model af proteiner fra sygdomsfremkaldende bakterier3D-strukturen af et enzym fra den sygdomsfremkaldende bakterie Streptococcus pneumoniae. Kredit:Canadisk lyskilde Millioner af mennesker er ramt af bakterien Streptococcus pneumoniae, som kan fo
Forskere analyserer 3-D-model af proteiner fra sygdomsfremkaldende bakterier3D-strukturen af et enzym fra den sygdomsfremkaldende bakterie Streptococcus pneumoniae. Kredit:Canadisk lyskilde Millioner af mennesker er ramt af bakterien Streptococcus pneumoniae, som kan fo -
 Nye teorier og materialer hjælper overgangen til ren energiIllustration, der fremhæver de tre former for katalyse, der er beskrevet i det nye studie. Kredit:Jason Drees / The Biodesign Institute ved Arizona State University For hver dag der går, den mørke
Nye teorier og materialer hjælper overgangen til ren energiIllustration, der fremhæver de tre former for katalyse, der er beskrevet i det nye studie. Kredit:Jason Drees / The Biodesign Institute ved Arizona State University For hver dag der går, den mørke -
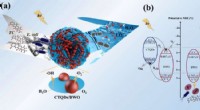 Forskere udvikler Z-skema katalysator for forurenende stoffer i vandSkematisk illustration af fotokatalytisk mekanisme. Kredit:YANG Pengqi I de seneste år, den hurtige industrialisering har forårsaget stadig mere alvorlig miljøforurening. Antibiotika og mikrobiolo
Forskere udvikler Z-skema katalysator for forurenende stoffer i vandSkematisk illustration af fotokatalytisk mekanisme. Kredit:YANG Pengqi I de seneste år, den hurtige industrialisering har forårsaget stadig mere alvorlig miljøforurening. Antibiotika og mikrobiolo -
 Tænd logik:Ingeniører udfører beregningslogik med lysSøjleformede flydende krystaller svarer i størrelse til nuværende halvledertransistorer. Kredit:(c)2019 Aida Group For første gang, forskere har udført logiske operationer med en kemisk enhed ved
Tænd logik:Ingeniører udfører beregningslogik med lysSøjleformede flydende krystaller svarer i størrelse til nuværende halvledertransistorer. Kredit:(c)2019 Aida Group For første gang, forskere har udført logiske operationer med en kemisk enhed ved
- Nye data om ultrahurtig elektronfotoemission fra metalliske nanostrukturer opnået
- Hvordan blodsugende insekter finder mørkbelagte kvæg i mørke
- Hvad er de to 2 trækkræfter?
- Har en 2 kg klippe dobbelt så meget som 1 kg sten?
- Hvad udløser amerikanske naturbrande:Elledninger, brændende affald og lyn
- Hvad sagde videnskabsbogen til Math Book?


