Hvordan sammenligner du og kontrasterer væsker faste stoffer?
Sammenligning og kontrast af væsker, faste stoffer og gasser:
Her er en oversigt over de vigtigste forskelle og ligheder mellem væsker, faste stoffer og gasser:
Nøgleegenskaber:
| Ejendom | Solid | Væske | Gas |
| --- | --- | --- | --- |
| form | Bestemt | Tager formen på sin beholder | Tager formen på sin beholder |
| volumen | Bestemt | Bestemt | Fylder hele volumenet af dens beholder |
| densitet | Høj | Moderat | Lav |
| Kompressibilitet | Meget lav | Meget lav | Høj |
| molekylær arrangement | Tæt pakket, regelmæssigt mønster | Tæt pakket, intet regelmæssigt mønster | Bredt fordelt, intet regelmæssigt mønster |
| molekylær bevægelse | Vibrerer i faste positioner | Vibrerer og oversæt tilfældigt | Vibrerer og oversæt hurtigt og tilfældigt |
| diffusion | Meget langsom | Langsommere end gasser | Meget hurtig |
| overfladespænding | Nuværende | Nuværende | Ikke relevant |
| Eksempler | Rock, is, metal | Vand, olie, kviksølv | Luft, ilt, helium |
Sammenligning:
* Matterilat: Alle tre stater findes på grund af de forskellige niveauer af tiltrækning og bevægelse mellem deres molekyler.
* densitet: Faststoffer er tættere end væsker, som er tættere end gasser. Dette skyldes, at molekylerne i faste stoffer pakkes tæt, mens de i gasser er fordelt langt fra hinanden.
* Kompressibilitet: Gasser komprimeres let, fordi deres molekyler er langt fra hinanden og kan presses tættere sammen. Faststoffer og væsker er næsten ukomprimerbare på grund af deres nære molekylære arrangement.
* Bevægelse: Molekylerne i et fast stof fastgøres i position og vibrerer. Væsker har molekyler, der bevæger sig frit og glider forbi hinanden. Gasser har mest bevægelse, med molekyler bevæger sig hurtigt og tilfældigt.
Kontrast:
* Form og volumen: Faststoffer har en fast form og volumen. Væsker har et fast volumen, men tag formen på deres beholder. Gasser har ingen fast form eller volumen.
* diffusion: Gasser diffunderer meget hurtigere end væsker, som diffunderer hurtigere end faste stoffer. Dette skyldes, at molekyler i gasser bevæger sig hurtigt og let kan passere gennem hinanden.
Vigtig note: Det er vigtigt at huske, at dette er generelle egenskaber, og der er undtagelser fra hver regel. For eksempel kan nogle faste stoffer være ret komprimerbare, og nogle væsker kan være meget tyktflydende (tyk).
Sammendrag: De forskellige egenskaber ved faste stoffer, væsker og gasser er direkte relateret til arrangementet og bevægelsen af deres molekyler. Denne grundlæggende forskel i molekylær opførsel giver hver tilstand af stof dens unikke egenskaber.
Sidste artikelHvordan finder ledning sted i metal?
Næste artikelEr fosfor en dirigent, eller er det en isolator?
 Varme artikler
Varme artikler
-
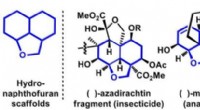 Vigtige tricykliske kemiske forbindelser med effektiv chiralitetskontrolFigur 1. Repræsentative eksempler på bioaktive molekyler med hydronaphthofurans stilladser. Kredit:Osaka University Osaka University-forskere udviklede en meget effektiv måde at producere chirale
Vigtige tricykliske kemiske forbindelser med effektiv chiralitetskontrolFigur 1. Repræsentative eksempler på bioaktive molekyler med hydronaphthofurans stilladser. Kredit:Osaka University Osaka University-forskere udviklede en meget effektiv måde at producere chirale -
 Video:Hvad er nordlyset?Kredit:The American Chemical Society Hver vinter, tusindvis af turister tager mod nord i håb om at få et glimt af de lysende nordlys, der danser på himlen. I denne episode af Reactions, Vi deler
Video:Hvad er nordlyset?Kredit:The American Chemical Society Hver vinter, tusindvis af turister tager mod nord i håb om at få et glimt af de lysende nordlys, der danser på himlen. I denne episode af Reactions, Vi deler -
 Forstå sprøde revner for at designe stærkere materialerKredit:CC0 Public Domain I et papir udgivet i Naturfysik , Northeastern University Department of Physics Arts and Sciences Distinguished Professor Alain Karma, i samarbejde med hans postdoktoral
Forstå sprøde revner for at designe stærkere materialerKredit:CC0 Public Domain I et papir udgivet i Naturfysik , Northeastern University Department of Physics Arts and Sciences Distinguished Professor Alain Karma, i samarbejde med hans postdoktoral -
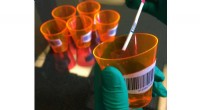 Påvisning af små mængder virus ved tidlige infektionerHøjtryks forkoncentrationsanordninger til at øge styrken af biovæskeprøver, der skal bruges med point-of-care assays til påvisning af patogener, såsom influenza eller coronavirus. Kredit:Amy Drexeli
Påvisning af små mængder virus ved tidlige infektionerHøjtryks forkoncentrationsanordninger til at øge styrken af biovæskeprøver, der skal bruges med point-of-care assays til påvisning af patogener, såsom influenza eller coronavirus. Kredit:Amy Drexeli
- Eksperimenter for at fuldende videnskabelig forståelse af, hvordan reduceret tyngdekraft påvirker …
- Hvad er de 3 naturlige blandinger, der findes på Jorden?
- Hvorfor er det vigtigt for ingeniører at kende og forstå de forskellige former for energi?
- Hvad er energitransformationen af en varm ballom?
- Hvad betyder saltkoncentration?
- Algoritme giver netværk den mest aktuelle information, der er tilgængelig, samtidig med at dataove…


