Vigtige tricykliske kemiske forbindelser med effektiv chiralitetskontrol
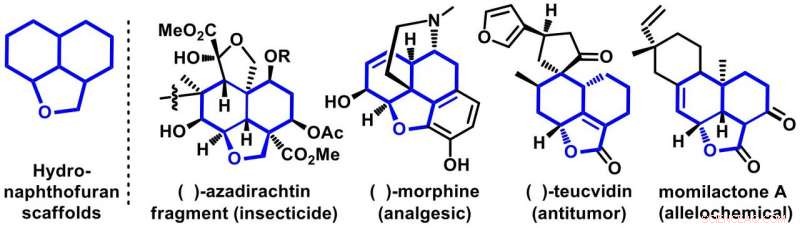
Figur 1. Repræsentative eksempler på bioaktive molekyler med hydronaphthofurans stilladser. Kredit:Osaka University
Osaka University-forskere udviklede en meget effektiv måde at producere chirale multi-centrerede fusionerede tricykliske forbindelser, hvis kernestruktur ofte findes i bioaktive forbindelser, herunder medicin.
Kemikere har viet en enorm indsats for at udvikle en måde at bygge molekyler på, som de vil. En enkelt enantiomer (specifik speciel arrangement af atomer) er essentiel for molekyler med specifikke biomedicinske egenskaber på grund af den chirale natur af biologiske receptorsteder (normalt proteiner). Et meget udfordrende mål inden for organisk kemi er asymmetrisk syntese, selektiv fremstilling af en enkelt enantiomer af et molekyle.
For nylig, kemikere ved Osaka University har syntetiseret meget enantioselektive polycykliske chirale forbindelser med flere chirale centre på en elegant og selektiv måde, der kunne åbne nye veje inden for forskning og industri.
I deres rapport i Naturkommunikation , Osaka-teamet fokuserede på at udvikle en ny og praktisk måde at syntetisere tricykliske molekyler på, kaldet hydronaphthofurans. Disse stilladser er rigelige af naturlige produkter af vigtige biologiske aktiviteter. De repræsentative medlemmer af denne familie er morfin, azadirachtin, teucvidin og momilacton, der er velkendte for at vise en række biologiske aktiviteter såsom smertestillende, anti-tumor, insekticider, og allelokemikalier (figur 1). Selvom nogle findes i naturen, at forberede dem i det syntetiske laboratorium med fuld kontrol over selektiviteten er en stor udfordring for de syntetiske kemikere.
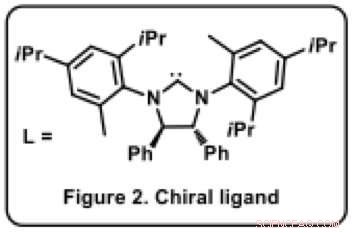
Figur 2. Chiral ligand. Kredit:Osaka University
En rapporteret syntese af en spansk gruppe brugte en organisk molekyle baseret chiral katalysator til at producere et tricyklisk stillads med tre chirale centre. På den anden side, Osaka-teamet vedtog en konceptuelt anderledes strategi for at bygge det tricykliske stillads med fem chirale centre (skema 1). Startende med et billigt råmateriale med kun én ring (phenoler), de brugte en organometallisk nikkel-baseret chiral katalysator til at konstruere yderligere to ringe gennem en reaktion kaldet oxidativ ringslutning (1 til 2). In situ fortrængning af nikkel fra et mellemprodukt 2 med et andet reaktivt molekyle af ønskede substituenter gav en række forskellige hydronaphthofuraner. Slutproduktet er dannet som en enkelt isomer, og som indeholdt mindst fem chirale centre, fordelt på alle tre ringe.
Ravindra Kumar, en af teammedlemmet forklarer, "Katalysatoren er nøglen til chiral selektivitet, da det er chiralt i sig selv." Faktisk, selvom anvendelsen af nikkelkatalysatorer er udbredt i organisk syntese, ingen havde brugt i denne reaktion før. "I en organometallisk katalysator, det er afgørende at vedhæfte en passende ligand [organisk molekyle, L*] til metalatomet for at bestemme reaktionsresultatet. Liganden er typisk et voluminøst organisk molekyle med flere ringsystemer (figur 2). I vores tilfælde, det var en proces med informeret trial-and-error at finde en passende ligand, der gav det ønskede produkt som en enkelt forbindelse (ud af mulige seksten) både i højt udbytte og med fremragende chiral renhed.
Med den passende katalysator i hånden, holdet producerede med succes over tyve forbindelser i gode udbytter og med 94 til 99 % enantioselektivitet af alle fem chirale centre – en spektakelpræstation! Tolerance af en lang række substituenter (R) (halogener, benzenringe og estere) i den udviklede metode og tilstedeværelsen af funktionaliserbare grupper (carbonyler og olefiner) udvider den potentielle syntetiske anvendelighed af tricykliske produkter til bioaktive molekyler efter funktionel gruppetransformation. Udover at tilbyde fremragende chiral renhed, reaktionen er også hurtig og økonomisk med hensyn til udgangsråvarer, som er afgørende krav for at opskalere forskningen fra laboratorie- til industriel produktion.
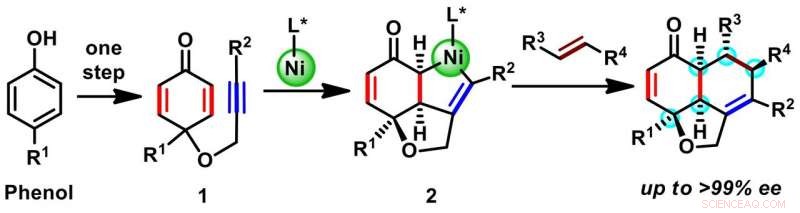
Skema 1. Totrins enantioselektiv syntese af hydronaphthofurans stilladser. Kredit:Osaka University
"Disse tricykliske produkter er traditionelt blevet fremstillet ved trinvis ringkonstruktion, men det plejer at være langsomt og ineffektivt, "Sensuke Ogoshi, teamdirektøren, siger. "Vores direkte to-trins cyklisering giver adgang til en række meget nyttige stilladser til naturlige produkter. På længere sigt, dette kunne ikke kun forenkle produktionen af kendt medicin, men måske føre til opdagelsen af nye forbindelser med medicinske eller andre biologiske egenskaber."
 Varme artikler
Varme artikler
-
 Et nyt paradigme for materialeidentifikation baseret på grafteoriDen forenklede graf og den faktiske krystalstruktur (øverst til højre) af spinel Co3O4. Kredit:Science China Press Materials Genome Initiative (MGI) og National Materials Genome Project er blevet
Et nyt paradigme for materialeidentifikation baseret på grafteoriDen forenklede graf og den faktiske krystalstruktur (øverst til højre) af spinel Co3O4. Kredit:Science China Press Materials Genome Initiative (MGI) og National Materials Genome Project er blevet -
 Styring af varmen åbner døren til næste generations belysning og displays i perovskit-LED'erPrinceton-forskere har forfinet fremstillingen af lysemitterende dioder fremstillet med krystallinske strukturer kendt som perovskitter, et mere effektivt og potentielt billigere alternativ til mate
Styring af varmen åbner døren til næste generations belysning og displays i perovskit-LED'erPrinceton-forskere har forfinet fremstillingen af lysemitterende dioder fremstillet med krystallinske strukturer kendt som perovskitter, et mere effektivt og potentielt billigere alternativ til mate -
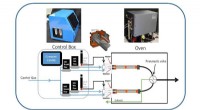 Spordampgenerator til detektering af sprængstoffer, narkotikaDiagram, der illustrerer analyttens flowvej i en vandig opløsning, når den bevæger sig fra prøveindføringsbeholderne på Trace Vapor Generator for Explosives and Narcotics (TV-Gen) kontrolboksen, genne
Spordampgenerator til detektering af sprængstoffer, narkotikaDiagram, der illustrerer analyttens flowvej i en vandig opløsning, når den bevæger sig fra prøveindføringsbeholderne på Trace Vapor Generator for Explosives and Narcotics (TV-Gen) kontrolboksen, genne -
 Kan sollys omdanne emissioner til nyttige materialer?Kredit:Pixabay/CC0 Public Domain Shaama Sharada kalder kuldioxid - den værste lovovertræder af den globale opvarmning - en meget stabil, meget glad molekyle. Det vil hun ændre på. For nylig off
Kan sollys omdanne emissioner til nyttige materialer?Kredit:Pixabay/CC0 Public Domain Shaama Sharada kalder kuldioxid - den værste lovovertræder af den globale opvarmning - en meget stabil, meget glad molekyle. Det vil hun ændre på. For nylig off
- Mulighed for misbrug af klimadata en trussel mod erhvervslivet og de finansielle markeder
- Forfiner billedet af Higgs boson
- Indonesien øger estimatet for skader på krydstogtskibe
- Guldnanopartikler:En ny levering til kræftmedicin
- At undervise i fysik til neurale netværk fjerner kaosblindhed
- Modellering viser et presserende behov for at forny ansættelses- og arbejdsforhold for astronomer


