Hvorfor udvides gasser mest ved opvarmning og faste stoffer mindst?
1. Intermolekylære kræfter:
* Gasser: Gasmolekyler er meget langt fra hinanden med meget svage intermolekylære kræfter. De bevæger sig frit og tilfældigt. Når de opvarmes, øges molekylernes kinetiske energi markant, hvilket får dem til at bevæge sig hurtigere og sprede sig yderligere. Dette fører til en stor ekspansion i volumen.
* væsker: Flydende molekyler er tættere sammen end gasmolekyler med stærkere intermolekylære kræfter. De kan stadig bevæge sig rundt, men deres bevægelse er mere begrænset. Opvarmning øger deres kinetiske energi, hvilket får dem til at bevæge sig hurtigere og sprede sig lidt, men de stærkere kræfter begrænser ekspansionen sammenlignet med gasser.
* faste stoffer: Faststoffer har de stærkeste intermolekylære kræfter, der holder molekyler i en fast, stiv struktur. Mens opvarmning øger vibrationen af molekyler inden for denne struktur, forhindrer de stærke kræfter dem i at bevæge sig langt fra hinanden. Således udvides faste stoffer mindst, når de opvarmes.
2. Densitet:
* Gasser: Gasser har den laveste tæthed, fordi deres molekyler er langt fra hinanden. Dette betyder, at der er mere plads til molekylerne til at sprede sig, når de opvarmes.
* væsker: Væsker har en højere densitet end gasser. Dette begrænser udvidelsen, da molekylerne har mindre plads til at bevæge sig.
* faste stoffer: Faststoffer har den højeste tæthed, hvilket betyder, at deres molekyler er tæt pakket. Dette efterlader lidt plads til ekspansion, når det opvarmes.
3. Termisk ekspansionskoefficient:
Den termiske ekspansionskoefficient er en materiel egenskab, der kvantificerer, hvor meget et materiale udvides for en given temperaturstigning. Gasser har den højeste koefficient, efterfulgt af væsker, og faste stoffer har den laveste.
Kortfattet:
Forskellen i ekspansion er direkte relateret til bevægelsesfriheden for molekyler inden for hver stofstilstand. Jo svagere de intermolekylære kræfter og jo lavere densitet er, jo større er udvidelsen efter opvarmning.
Sidste artikelHvorfor bliver gasser ledere ved lavt tryk og højspænding?
Næste artikelHvad er produktet af Alpha Decay RN-220?
 Varme artikler
Varme artikler
-
 Forskere fanger øjeblikke med spirende krystaldannelse og vækstFoto af en guldkrystal. Kredit:© Paul Straathof/Pauls Lab Omdannelse af de fleste materialer til organiseret krystallinsk struktur starter med nukleationsprocessen. Et daglig eksempel er den hurti
Forskere fanger øjeblikke med spirende krystaldannelse og vækstFoto af en guldkrystal. Kredit:© Paul Straathof/Pauls Lab Omdannelse af de fleste materialer til organiseret krystallinsk struktur starter med nukleationsprocessen. Et daglig eksempel er den hurti -
 Musling-inspirerede belægninger til levering af lægemidlerKredit:CC0 Public Domain Naturen er fuld af vidunderlige, gennemprøvede løsninger på forskellige udfordringer. Videnskaben har vendt sin opmærksomhed mod at reproducere og genbruge disse fænomener
Musling-inspirerede belægninger til levering af lægemidlerKredit:CC0 Public Domain Naturen er fuld af vidunderlige, gennemprøvede løsninger på forskellige udfordringer. Videnskaben har vendt sin opmærksomhed mod at reproducere og genbruge disse fænomener -
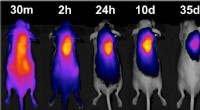 Et hyppelys for kemoterapilægemidlerHos mus, en hydrogel rekrutterer et farvestoffemærket molekyle (farvede områder) til sin placering, viser dets potentiale til at være et hjemfyrtårn for kræftmedicin. Kredit:Tilpasset fra ACS Central
Et hyppelys for kemoterapilægemidlerHos mus, en hydrogel rekrutterer et farvestoffemærket molekyle (farvede områder) til sin placering, viser dets potentiale til at være et hjemfyrtårn for kræftmedicin. Kredit:Tilpasset fra ACS Central -
 Forskere har fundet en måde at skabe lægemiddelmolekyler ud fra kulilteResultaterne af atomeffektivitetsreaktioner. Kredit:Denis Chusov Forskere fra RUDN Universitet har i samarbejde med russiske og udenlandske kolleger studeret reduktive amineringsreaktioner. De nye
Forskere har fundet en måde at skabe lægemiddelmolekyler ud fra kulilteResultaterne af atomeffektivitetsreaktioner. Kredit:Denis Chusov Forskere fra RUDN Universitet har i samarbejde med russiske og udenlandske kolleger studeret reduktive amineringsreaktioner. De nye
- Hvilken slags tidsskrift giver indsendelser til eksterne forskere, der læser og kommenterer?
- Hvordan produceres varmeenergi af friktion?
- Hvor krydret bliver sennep afhængigt af jorden?
- Nanorør transistor styret af ATP kunne forbedre menneske-maskine kommunikation
- At give en stemme til indvandrermødre fra Latina, der er ramt af COVID-19
- En træblok frigøres fra hvile øverst på en friktionsfri tilbøjelig plan og glider ned til bund …


