Hvilket princip tillader, at kalorimetri bruges til at bestemme den specifikke varmekapacitet af et stof?
Sådan fungerer det:
* kalorimetri: Kalorimetri involverer måling af varmestrømmen ind i eller ud af et system. Dette gøres ved at placere stoffet i et kalorimeter (en enhed designet til at isolere og måle varmeoverførsel).
* Specifik varmekapacitet: Specifik varmekapacitet er den mængde varme, der kræves for at hæve temperaturen på 1 gram af et stof med 1 graders celsius (eller kelvin).
* Energibesparelse: Det grundlæggende princip siger, at energi ikke kan skabes eller ødelægges, kun overføres eller transformeres.
Hvordan kalorimetri fungerer:
1. Varmeoverførsel: Når et stof opvarmes eller afkøles, udveksler det varme med dets omgivelser (kalorimeteret og dets indhold). Denne varmeoverførsel måles ved hjælp af kalorimeteret.
2. Energibalance: Den varme, der er opnået af stoffet, er lig med den varme, der går tabt af omgivelserne (og vice versa). Dette er baseret på bevarelse af energi.
3. Beregning: Ved at kende stoffets masse, temperaturændringen og den varme, der er absorberet eller frigivet (målt ved kalorimeteret), kan vi beregne den specifikke varmekapacitet ved hjælp af følgende ligning:
q =m * c * ΔT
Hvor:
* q er varmen absorberet eller frigivet (i Joules)
* m er massen af stoffet (i gram)
* C er den specifikke varmekapacitet (i J/G ° C)
* ΔT er temperaturændringen (i ° C)
Kortfattet: Calorimetry er afhængig af bevarelse af energi for at måle varmestrømmen, som derefter bruges til at beregne den specifikke varmekapacitet af et stof baseret på dets masse, temperaturændring og den målte varmeoverførsel.
Sidste artikelHvad er processen med at opdele atom kaldet?
Næste artikelHvad er erklæringen om lovfotokemisk ækvivalens?
 Varme artikler
Varme artikler
-
 Grønne kemikere finder en måde at gøre cashewnøddeskaller til solcremeEn grafisk fremstilling af det internationale samarbejde for at finde bæredygtige løsninger til fremstilling af nyttige forbindelser. Kredit:Wits University Et team af internationale forskere har
Grønne kemikere finder en måde at gøre cashewnøddeskaller til solcremeEn grafisk fremstilling af det internationale samarbejde for at finde bæredygtige løsninger til fremstilling af nyttige forbindelser. Kredit:Wits University Et team af internationale forskere har -
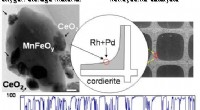 Ny katalysatorkomposit reducerer brugen af sjældne jordarterEn nyudviklet katalysator fra Japan, CeO2/MnFeOy, har både hurtig frigivelse og store opbevaringsmuligheder for ilt. Dens høje ydeevne i konverteringshastigheden af NOx, CO, og total kulbrinte til m
Ny katalysatorkomposit reducerer brugen af sjældne jordarterEn nyudviklet katalysator fra Japan, CeO2/MnFeOy, har både hurtig frigivelse og store opbevaringsmuligheder for ilt. Dens høje ydeevne i konverteringshastigheden af NOx, CO, og total kulbrinte til m -
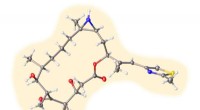 Lab skaber hårde, men øm, kræftkæmpereStruktur af en af analogerne til epothilon B, en ny forbindelse oprettet i Rice University lab af syntetisk organisk kemiker K.C. Nicolaou, der viser løfte som kræftkæmper. Kredit:Nicolaou Group/Ric
Lab skaber hårde, men øm, kræftkæmpereStruktur af en af analogerne til epothilon B, en ny forbindelse oprettet i Rice University lab af syntetisk organisk kemiker K.C. Nicolaou, der viser løfte som kræftkæmper. Kredit:Nicolaou Group/Ric -
 Ny forskning identificerer Fukushima -reaktormateriale i miljøetEt 3D-billede, der tillod forskerne at opdage fordelingen af elementer i prøven. Kredit:University of Bristol/Diamond Light Source Gennem analyse af specifikke nedfaldspartikler i miljøet, et fæ
Ny forskning identificerer Fukushima -reaktormateriale i miljøetEt 3D-billede, der tillod forskerne at opdage fordelingen af elementer i prøven. Kredit:University of Bristol/Diamond Light Source Gennem analyse af specifikke nedfaldspartikler i miljøet, et fæ
- Hvordan får detritivorer energi?
- ORNL producerer sjælden ruthenium -isotop til atomsprøjtningseksperiment
- Økologisk strømlagringsbatteri lavet af vanillin
- Hvorfor søfarende pattedyr skal være større end jordsmækkere
- Typer af sfæriske spejle
- For fem år siden introducerede Amazon Alexa. Navnet bliver måske aldrig det samme. Her er hvad der…


