Hvad gør Atom reaktiv?
Hvad gør atomer reaktive?
Atomer er reaktive, fordi de stræber efter at opnå en stabil elektronkonfiguration. Dette betyder at have en fuld ydre skal af elektroner. Her er hvorfor:
* Elektronkonfiguration: Elektroner kredserer kernen i et atom i specifikke energiniveauer kaldet skaller. Den yderste skal kaldes valensskallen, og dens elektroner er involveret i kemisk binding.
* stabilitet: Atomer er mest stabile, når deres valensskal er fuld. En fuld valensskal betyder, at atomet har det mest gunstige arrangement af elektroner, der minimerer dens energi.
* octet regel: Atomer har en tendens til at vinde, miste eller dele elektroner for at opnå en fuld ydre skal af 8 elektroner (med et par undtagelser, som brint og helium, som kun har brug for 2).
Hvordan reaktivitet opstår
* ufuldstændige valensskaller: Atomer med ufuldstændige valensskaller er reaktive. De vil let danne bindinger med andre atomer for at vinde, miste eller dele elektroner og opnå en stabil konfiguration.
* Elektronegativitet: Elektronegativitet er et mål for et atoms evne til at tiltrække elektroner. Atomer med høj elektronegativitet tiltrækker kraftigt elektroner, mens de med lav elektronegativitet ikke gør det. Forskellen i elektronegativitet mellem to atomer påvirker den type binding, de vil danne (ionisk eller kovalent).
Eksempler på reaktivitet
* natrium (NA): Natrium har en elektron i sin valensskal. Det mister let dette elektron for at opnå en stabil konfiguration og bliver en positivt ladet ion (Na+).
* klor (Cl): Klor har syv elektroner i sin valensskal. Det får let et elektron for at afslutte sin ydre skal og blive en negativt ladet ion (CL-).
* ilt (O): Oxygen har seks elektroner i sin valensskal. Det kan få to elektroner til at danne en oxidion (O2-) eller dele to elektroner med et andet atom til at danne en kovalent binding.
Nøglepunkter
* reaktivitet er relativ: Nogle atomer er mere reaktive end andre.
* binding: Atomer reagerer på dannelsesbindinger (ioniske, kovalente eller metalliske) for at opnå stabilitet.
* Periodiske tendenser: Reaktivitet påvirkes af faktorer som elektronegativitet og ioniseringsenergi, der viser tendenser inden for den periodiske tabel.
Fortæl mig, hvis du gerne vil have en mere dybdegående forklaring af et specifikt aspekt af atomreaktivitet!
 Varme artikler
Varme artikler
-
 Forskere opdager nye og skadelige kobber-proteinkomplekserKredit:TU Delft Kobber er vigtigt for mange processer i vores krop. Det understøtter produktionen af røde blodlegemer, stofskifte, og dannelsen af bindevæv og knogler, blandt andet. Kobber er
Forskere opdager nye og skadelige kobber-proteinkomplekserKredit:TU Delft Kobber er vigtigt for mange processer i vores krop. Det understøtter produktionen af røde blodlegemer, stofskifte, og dannelsen af bindevæv og knogler, blandt andet. Kobber er -
 Ny indsigt i nanokrystalvækst i væskeGlimmer mineralet flager af i fine plader. Kredit:Wikimedia Commons Mange muslingeskaller, mineraler, og halvleder nanomaterialer er opbygget af mindre krystaller, som er samlet som brikkerne i et
Ny indsigt i nanokrystalvækst i væskeGlimmer mineralet flager af i fine plader. Kredit:Wikimedia Commons Mange muslingeskaller, mineraler, og halvleder nanomaterialer er opbygget af mindre krystaller, som er samlet som brikkerne i et -
 Ny måleteknik kan spare pulpfabrikker millionerKredit:CC0 Public Domain Ny forskning ved Karlstad Universitet viser, at pulpfabrikker kan spare millioner ved at bruge en ny måleteknik. Denne nye teknik muliggør kontrol af pulpningsprocessen, h
Ny måleteknik kan spare pulpfabrikker millionerKredit:CC0 Public Domain Ny forskning ved Karlstad Universitet viser, at pulpfabrikker kan spare millioner ved at bruge en ny måleteknik. Denne nye teknik muliggør kontrol af pulpningsprocessen, h -
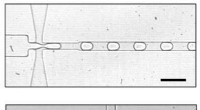 På vej til en kunstig celleCeller lavet af vand i olie:Ved hjælp af mikrofluidikteknologi, et fransk-tysk forskerhold genererer først små dråber (øverst), hvori komponenterne i et simpelt stofskifte derefter injiceres (nederst)
På vej til en kunstig celleCeller lavet af vand i olie:Ved hjælp af mikrofluidikteknologi, et fransk-tysk forskerhold genererer først små dråber (øverst), hvori komponenterne i et simpelt stofskifte derefter injiceres (nederst)
- Virksomheder med eksklusive netværk udmærker sig med 7 % i markedskriser:Undersøgelse
- At rette byers vandkrise kan sende vores klimamål ned i gurgleren
- Hvad siger du, at kemi lever hjemme?
- Hvad forårsagede emissionskode P0302 på 01 Mercury Mystique?
- Når acceleration og hastighedsvektorer peger i modsatte retninger?
- Muliggør kulstoffangst, brug og opbevaring


