Hvordan hjælper et enzym en reaktion forekommer?
1. Sænkning af aktiveringsenergien:
* Hver kemisk reaktion kræver en vis mængde energi for at komme i gang, kaldet aktiveringsenergi.
* Enzymer giver en alternativ reaktionsvej med en lavere aktiveringsenergi. Dette gør det lettere for reaktanterne at nå overgangstilstanden og danne produkter.
2. Tilvejebringelse af et specifikt bindingssted:
* Enzymer har en unik tredimensionel struktur med et specifikt aktivt sted, der binder til reaktanterne (substrater).
* Det aktive sted er komplementært i form og ladning til underlaget, hvilket muliggør præcis interaktion og dannelse af et enzym-substratkompleks.
3. Stabilisering af overgangstilstanden:
* Når den er bundet til det aktive sted, hjælper enzymet med at stabilisere overgangstilstanden, som er den ustabile mellemform af underlaget.
* Denne stabilisering sænker aktiveringsenergien og øger reaktionshastigheden.
4. Orientering af reaktanter:
* Enzymer bringer reaktanterne sammen i den korrekte orientering for, at reaktionen forekommer.
* Denne nærhed og korrekt positionering letter dannelsen af obligationer eller brud på obligationer.
5. Tilvejebringelse af et surt eller grundlæggende miljø:
* Nogle enzymer bruger aminosyrerester på deres aktive steder for at tilvejebringe et surt eller grundlæggende miljø, der fremmer reaktionen.
* Dette muliggør overførsel af protoner eller elektroner, som er nødvendige for visse kemiske transformationer.
I resumé accelererer enzymer kemiske reaktioner ved:
* Sænkning af aktiveringsenergien
* Tilvejebringelse af et specifikt bindingssted
* Stabilisering af overgangstilstanden
* Orientering af reaktanter
* Tilvejebringelse af et surt eller grundlæggende miljø
Denne katalytiske aktivitet er afgørende for utallige biokemiske processer, der opretholder livet, såsom fordøjelse, respiration, DNA -replikation og proteinsyntese.
 Varme artikler
Varme artikler
-
 Lovende ny soldrevet vej til brintbrændstofproduktionLeah C. Spangler udfører et eksperiment i Lehighs Health Research Hub. Kredit:Ryan Hulvat Ingeniører ved Lehigh University er de første til at udnytte en enkelt enzym biomineraliseringsproces til
Lovende ny soldrevet vej til brintbrændstofproduktionLeah C. Spangler udfører et eksperiment i Lehighs Health Research Hub. Kredit:Ryan Hulvat Ingeniører ved Lehigh University er de første til at udnytte en enkelt enzym biomineraliseringsproces til -
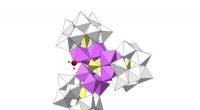 Kobolt og wolfram - nøglen til billigere, renere brintDen nye katalysator splitter vandmolekyler for at opnå brint og oxygen med meget lave spændinger. Kredit:ICIQ Elektrolyse, spaltning af vandmolekyler med elektricitet, er den reneste måde at få br
Kobolt og wolfram - nøglen til billigere, renere brintDen nye katalysator splitter vandmolekyler for at opnå brint og oxygen med meget lave spændinger. Kredit:ICIQ Elektrolyse, spaltning af vandmolekyler med elektricitet, er den reneste måde at få br -
 Stilladsmetoden gør det muligt for biokemikere at se proteiner i bemærkelsesværdige detaljerForskning fra UCLAs Tamir Gonen, venstre, Todd Yeates og Yuxi Liu, sammen med UCSFs Shane Gonen (ikke vist), giver værdifuld indsigt i komponenter i cellen. Kredit:Reed Hutchinson/UCLA UCLA-biokem
Stilladsmetoden gør det muligt for biokemikere at se proteiner i bemærkelsesværdige detaljerForskning fra UCLAs Tamir Gonen, venstre, Todd Yeates og Yuxi Liu, sammen med UCSFs Shane Gonen (ikke vist), giver værdifuld indsigt i komponenter i cellen. Kredit:Reed Hutchinson/UCLA UCLA-biokem -
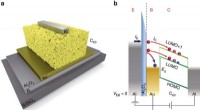 Marcus regime i organiske enheder - grænsefladeladningsoverførselsmekanisme verificeretEnhedsskemaer. a – Skematisk tværsnit af enheden. b – Varmelektrontransistordrift. Elektroner injiceres ved at anvende en negativ emitter-base bias, og detekteret i den molekylære halvleder. Disse ele
Marcus regime i organiske enheder - grænsefladeladningsoverførselsmekanisme verificeretEnhedsskemaer. a – Skematisk tværsnit af enheden. b – Varmelektrontransistordrift. Elektroner injiceres ved at anvende en negativ emitter-base bias, og detekteret i den molekylære halvleder. Disse ele
- Er mekanisk energi en vektorkvalitet?
- Giv et eksempel på, hvordan termisk ekspansion er blevet brugt til godt og klogt forvaltning i verd…
- Hvad er en stødende klippe med små krystaller kaldet?
- Hvad betyder halvtørret?
- Tværbundne hultransportlag til højeffektive perovskit tandem solceller
- Nissan ramt af ny inspektionsskandale efter Ghosn-anholdelse:rapport


