Hvad er vandmolekyler polære med?
Her er hvorfor:
* ilt er mere elektronegativ: Oxygen har et stærkere træk på elektroner end brint. Dette betyder, at de delte elektroner i O-H-bindingerne bruger mere tid tættere på iltatomet.
* ujævn gebyrfordeling: Oxygenatomet ender med en lidt negativ ladning (Δ-), fordi det har en højere elektrondensitet. Hydrogenatomerne, efter at have mistet en vis elektrondensitet, bliver lidt positive (δ+).
* dipolmoment: Denne ujævne fordeling af ladning skaber et dipolmoment, hvor den positive slutning peger mod hydrogenatomerne og det negative slutning, der peger mod iltatomet.
Denne polaritet tillader vandmolekyler at danne hydrogenbindinger med hinanden og med andre polære molekyler, hvilket er afgørende for mange af dens egenskaber, som dets høje kogepunkt, overfladespænding og evne til at opløse mange stoffer.
 Varme artikler
Varme artikler
-
 Nysyntetiseret AM-III kulstof er det hårdeste og stærkeste amorfe materiale til datoHårdhed af AM carbon materialer, sammenlignet med andre kendte amorfe materialer, og ridser på diamant (001) flade indtrukket af AM-III. Kredit: National Science Review (2021). DOI:10.1093/nsr/nwab14
Nysyntetiseret AM-III kulstof er det hårdeste og stærkeste amorfe materiale til datoHårdhed af AM carbon materialer, sammenlignet med andre kendte amorfe materialer, og ridser på diamant (001) flade indtrukket af AM-III. Kredit: National Science Review (2021). DOI:10.1093/nsr/nwab14 -
 Forskere finder frustration i batterimaterialerKunstnergengivelse af det faste elektrolytmateriale, viser lithium-atomer (lilla) bevæger sig inden for en matrix af anioner sammensat af bor (grøn), kulstof (grå) og brint (hvid) atomer. Kredit:Joel
Forskere finder frustration i batterimaterialerKunstnergengivelse af det faste elektrolytmateriale, viser lithium-atomer (lilla) bevæger sig inden for en matrix af anioner sammensat af bor (grøn), kulstof (grå) og brint (hvid) atomer. Kredit:Joel -
 Hvordan blækspruttecamouflage kan hjælpe med at forhindre hudkræft hos menneskerEt team af nordøstlige forskere bruger kemien i blækspruttehud til at skabe en bærbar enhed, der registrerer skadelige niveauer af UV-stråling. Kredit:Alyssa Stone/Northeastern University Det var i
Hvordan blækspruttecamouflage kan hjælpe med at forhindre hudkræft hos menneskerEt team af nordøstlige forskere bruger kemien i blækspruttehud til at skabe en bærbar enhed, der registrerer skadelige niveauer af UV-stråling. Kredit:Alyssa Stone/Northeastern University Det var i -
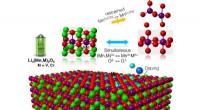 Forskere forudser materialer til at stabilisere et lithium-ion-batteri med rekordhøj kapacitetEn skematisk illustration af batteriets katodestruktur, hvor litium er rødt, ilt er grønt, mangan er lilla, krom er mørkeblå og vanadium er lyseblå. Kredit:Wolverton Research Group, Northwestern Unive
Forskere forudser materialer til at stabilisere et lithium-ion-batteri med rekordhøj kapacitetEn skematisk illustration af batteriets katodestruktur, hvor litium er rødt, ilt er grønt, mangan er lilla, krom er mørkeblå og vanadium er lyseblå. Kredit:Wolverton Research Group, Northwestern Unive


