Hvorfor blev der anvendt en koncentreret løsning, hvis der ikke var nogen reaktion med den fortyndede løsning?
* Forøget koncentration betyder mere reaktant: En koncentreret opløsning pakker flere reaktantmolekyler i det samme volumen. Dette kan:
* overvinde aktiveringsenergi: Nogle reaktioner har brug for en bestemt minimumsmængde energi for at starte. En koncentreret løsning giver flere kollisioner og derfor en større chance for at nå dette energibehov.
* drev ligevægt: Selv hvis reaktionen er reversibel, kan en koncentreret opløsning skifte ligevægt mod produktsiden ved at tilvejebringe en højere initialkoncentration af reaktanten.
* opløselighedsbegrænsninger: Nogle gange er den reaktant, du har brug for at arbejde med, simpelthen mindre opløselig i opløsningsmidlet. Brug af en koncentreret løsning giver dig mulighed for at bruge en højere mængde af reaktanten uden at overskride dens opløselighedsgrænse.
* Test for satsafhængighed: Selv hvis der ikke er nogen observerbar reaktion med en fortyndet opløsning, kan du se, om reaktionshastigheden stiger markant med en koncentreret opløsning. Dette kan hjælpe dig med at forstå reaktionsmekanismen og identificere det hastighedsbegrænsende trin.
* Detektionsfølsomhed: En reaktion kan forekomme, men produktdannelsen kan være for lav til at detektere med den fortyndede opløsning. Brug af en koncentreret løsning kan øge mængden af dannet produkt, hvilket gør det lettere at registrere og analysere.
Vigtig note: Det er vigtigt at være forsigtig, når man arbejder med koncentrerede løsninger, da de kan være mere farlige på grund af deres højere reaktivitet og potentiale for eksoterme reaktioner.
Fortæl mig, hvis du har en bestemt reaktion i tankerne. Jeg kan muligvis give mere skræddersyede forklaringer!
 Varme artikler
Varme artikler
-
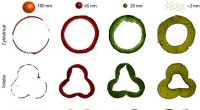 Fluorescerende alkometer gør optimering af katalysatorer meget nemmereFluorescensmikroskopibilleder viser virkningerne af forskellige former på katalysatoraktivitet. Kredit:Utrecht University En ny test for industrielle katalysatorer udviklet af kemikere ved Utrecht
Fluorescerende alkometer gør optimering af katalysatorer meget nemmereFluorescensmikroskopibilleder viser virkningerne af forskellige former på katalysatoraktivitet. Kredit:Utrecht University En ny test for industrielle katalysatorer udviklet af kemikere ved Utrecht -
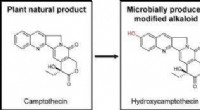 Mikrober kunne gøre medicinproduktionen mere effektivAlkaloidbaserede lægemidler afledt af planter kan være potente behandlinger for en række forskellige sygdomme. Men at få disse kraftfulde terapeutiske midler fra planter kan tage lang tid og koste man
Mikrober kunne gøre medicinproduktionen mere effektivAlkaloidbaserede lægemidler afledt af planter kan være potente behandlinger for en række forskellige sygdomme. Men at få disse kraftfulde terapeutiske midler fra planter kan tage lang tid og koste man -
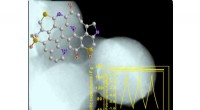 Højt nitrogen og svovl dobbelt-dopede kulstofmikrosfærer til superkondensatorerDenne figur viser morfologien, molekylær model og cyklisk ydeevne af den N/S co-doterede kulstofmikrosfære. Kredit:©Science China Press Blandt elektrodematerialer til superkondensatorer, kulstofba
Højt nitrogen og svovl dobbelt-dopede kulstofmikrosfærer til superkondensatorerDenne figur viser morfologien, molekylær model og cyklisk ydeevne af den N/S co-doterede kulstofmikrosfære. Kredit:©Science China Press Blandt elektrodematerialer til superkondensatorer, kulstofba -
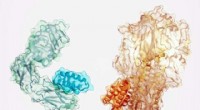 Ny metode til at generere potente, specifikke bindingsproteiner til nye lægemidlerSmå proteiner (mørkere nuance) designet til at binde sig til insulinreceptoren (venstre) og en komponent af influenzavirussen (højre). Kredit:Ian C. Haydon/Institute for Protein Design Et team af v
Ny metode til at generere potente, specifikke bindingsproteiner til nye lægemidlerSmå proteiner (mørkere nuance) designet til at binde sig til insulinreceptoren (venstre) og en komponent af influenzavirussen (højre). Kredit:Ian C. Haydon/Institute for Protein Design Et team af v
- Hvad er nogle elementer fremstillet af kulstof?
- Har NASA sendt en sonde eller satellit til solen?
- Hvordan interagerer Pluto med planeter?
- Hvor mange forskellige typer celler indeholder din krop?
- Hvad er den livsaktivitet, som organismer får og behandler mad?
- Hvad er større atomradius for kalium eller jod?


