Effekten af substratkoncentration på hastighedsreaktionen H202 og katalase?
Effekten af substratkoncentration på reaktionshastigheden af H2O2 og katalase
Reaktionen mellem hydrogenperoxid (H2O2) og katalase er et klassisk eksempel på enzymkinetik. Catalase, et enzym, der findes i næsten alle levende organismer, katalyserer nedbrydningen af H2O2 til vand (H2O) og ilt (O2).
Her er, hvordan substratkoncentration påvirker reaktionshastigheden:
1. Den oprindelige stigning i sats:
* Ved lave substratkoncentrationer øges reaktionshastigheden proportionalt med stigende H2O2 -koncentration. Dette skyldes, at der er flere substratmolekyler til rådighed for at binde til de aktive steder i katalaseenzymet.
* Dette er første orden Kinetikregion, hvor reaktionshastigheden er direkte proportional med substratkoncentrationen.
2. Mætningspunkt:
* Når substratkoncentrationen øges yderligere, er reaktionshastigheden til sidst plateauer. Dette skyldes, at alle de aktive steder i katalaseenzymet bliver mættet med H2O2 -molekyler.
* Selv hvis der tilsættes mere H2O2, vil reaktionshastigheden ikke stige, fordi enzymet ikke kan binde mere underlag.
3. Nulordre kinetik:
* Ved meget høje substratkoncentrationer bliver reaktionshastigheden uafhængig af substratkoncentrationen. Dette skyldes, at enzymet fungerer ved dets maksimale kapacitet, og at tilføje mere underlag vil ikke øge hastigheden.
* Dette er nulordren Kinetics -region.
Faktorer, der påvirker mætningspunktet:
* enzymkoncentration: En højere enzymkoncentration øger mætningspunktet, da der vil være mere aktive steder til rådighed til binding.
* Temperatur: Optimal temperatur øger reaktionshastigheden, men kan også denaturere enzymet. Højere temperaturer kan flytte mætningspunktet til højere substratkoncentrationer.
* ph: Hvert enzym har en optimal pH for aktivitet. Afvigelse fra den optimale pH kan reducere enzymets effektivitet og skifte mætningspunkt.
grafisk:
Forholdet mellem substratkoncentration og reaktionshastighed kan visualiseres med en graf:
* x-akse: Substratkoncentration (H2O2)
* y-akse: Reaktionshastighed (mængden af produkt dannet pr. Enhedstid)
Grafen viser en karakteristisk kurve, oprindeligt stigende stejlt og derefter plateauing ved mætningspunktet.
Betydning:
At forstå effekten af substratkoncentration på reaktionshastigheden er afgørende for:
* Forståelse af enzymkinetik: Denne viden hjælper os med at studere enzymfunktion, mekanisme og regulering.
* Optimering af enzymatiske reaktioner: Ved at justere substratkoncentrationen kan vi optimere reaktionshastigheden for specifikke anvendelser.
* Modellering af biologiske processer: Denne viden er afgørende for at forstå enzymernes opførsel i levende organismer.
I resumé øges reaktionshastigheden mellem H2O2 og katalase oprindeligt proportionalt med stigende substratkoncentration, derefter plateauer ved mætningspunktet og bliver til sidst uafhængig af substratkoncentrationen i meget høje koncentrationer. Dette forhold er afgørende for at forstå enzymkinetik og optimere enzymatiske reaktioner.
 Varme artikler
Varme artikler
-
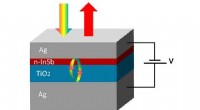 Forskere kommer på forbrugernes bølgelængde med InSb-teknologiSkematisk struktur af en elektrisk indstillelig perfekt lysabsorber. Teknologien til styring af lysabsorption ved udvalgte bølgelængder i nanostrukturer har fået stor opmærksomhed i de senere år;
Forskere kommer på forbrugernes bølgelængde med InSb-teknologiSkematisk struktur af en elektrisk indstillelig perfekt lysabsorber. Teknologien til styring af lysabsorption ved udvalgte bølgelængder i nanostrukturer har fået stor opmærksomhed i de senere år; -
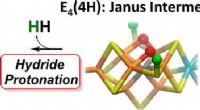 Sætter scenen for brændstofeffektiv gødningKredit:ACS Ammoniak, den primære ingrediens i nitrogenbaserede gødninger, har hjulpet med at brødføde verden siden 1. Verdenskrig. Men at lave ammoniak i industriel skala kræver meget energi, og d
Sætter scenen for brændstofeffektiv gødningKredit:ACS Ammoniak, den primære ingrediens i nitrogenbaserede gødninger, har hjulpet med at brødføde verden siden 1. Verdenskrig. Men at lave ammoniak i industriel skala kræver meget energi, og d -
 4-D printet termit kunne gøre svejsning i rummet og kampzoner lettere, sikrereNeelys har svejst jern (ovenfor) og kobber med den 4D-printede termitpasta. Kredit:Vanderbilt University En nyuddannet maskiningeniør har skabt et materiale til svejsning under ekstreme forhold, s
4-D printet termit kunne gøre svejsning i rummet og kampzoner lettere, sikrereNeelys har svejst jern (ovenfor) og kobber med den 4D-printede termitpasta. Kredit:Vanderbilt University En nyuddannet maskiningeniør har skabt et materiale til svejsning under ekstreme forhold, s -
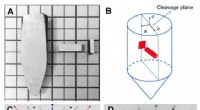 Høj termoelektrisk ydeevne i billige SnS0.91Se0.09-krystaller(A) En typisk krystal spaltet langs (100) planet, og prøve skåret langs b-aksen. (B) Et diagram viser, hvordan prøver skærer langs b-aksen til målinger. (C) Standard Laue diffraktionsbillede af SnS kr
Høj termoelektrisk ydeevne i billige SnS0.91Se0.09-krystaller(A) En typisk krystal spaltet langs (100) planet, og prøve skåret langs b-aksen. (B) Et diagram viser, hvordan prøver skærer langs b-aksen til målinger. (C) Standard Laue diffraktionsbillede af SnS kr
- Hvad menes med et kontrolleret eksperiment?
- Hvordan skriver du 5,2 millioner i videnskabelig notation?
- Oversvømmelse:Er det på tide at stoppe med at bo i kældre?
- Hvad er et andet navn på vævsrespiration?
- Hvad er forskellen mellem energikonvertering, der finder sted i en elektrisk motor med en generator?…
- Hvad laver NH3 og HCl?


