Den ulige deling af elektroner i et molekylevand er et eksempel på?
Her er hvorfor:
* kovalent binding: I kovalent binding deler atomer elektroner for at opnå en stabil elektronkonfiguration.
* polær: I en polær kovalent binding deles elektronerne ikke lige mellem atomerne. Dette sker, fordi det ene atom har en højere elektronegativitet (et stærkere træk på elektroner) end den anden.
* Vandmolekyle: Oxygen har en højere elektronegativitet end brint. Dette betyder, at de delte elektroner bruger mere tid tættere på iltatomet, hvilket giver det en delvis negativ ladning (Δ-) og forlader brintatomerne med delvis positive ladninger (Δ+).
Denne ulige deling af elektroner skaber et polært molekyle med en positiv afslutning (brintsiden) og en negativ ende (iltsiden). Denne polaritet er ansvarlig for mange af vandets unikke egenskaber, som dens evne til at danne brintbindinger og fungere som et godt opløsningsmiddel.
Sidste artikelHvad har et molekyle, der er blevet oxideret?
Næste artikelHvordan påvirker varme enzymerne i en kemisk reaktion?
 Varme artikler
Varme artikler
-
 På jagt efter stabile væskerDette kort er baseret på et Copernicus Sentinel-2-billede erhvervet den 11. august 2020 og giver en analyse af det seneste olieudslip i Mauritius. I juli, et olieskib gik på grund på koralrevet ud for
På jagt efter stabile væskerDette kort er baseret på et Copernicus Sentinel-2-billede erhvervet den 11. august 2020 og giver en analyse af det seneste olieudslip i Mauritius. I juli, et olieskib gik på grund på koralrevet ud for -
 Prober kaster nyt lys over Alzheimers årsagRice University-forskere har udviklet et rutheniumbaseret kompleks, der er i stand til at spore dannelsen af opløselige amyloide beta-peptidaggregater, der er impliceret i starten af Alzheimers sy
Prober kaster nyt lys over Alzheimers årsagRice University-forskere har udviklet et rutheniumbaseret kompleks, der er i stand til at spore dannelsen af opløselige amyloide beta-peptidaggregater, der er impliceret i starten af Alzheimers sy -
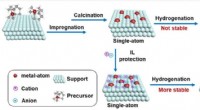 Forskere udvikler strategi for at stabilisere enkelte atomer med ionisk væske som elektronisk stabi…En skematisk illustration af forberedelsen af SACer og stabiliseringen af ILer. Kredit:DING Shiping Understøttede enkeltatomkatalysatorer (SACer) er dukket op som en ny grænse inden for hetero
Forskere udvikler strategi for at stabilisere enkelte atomer med ionisk væske som elektronisk stabi…En skematisk illustration af forberedelsen af SACer og stabiliseringen af ILer. Kredit:DING Shiping Understøttede enkeltatomkatalysatorer (SACer) er dukket op som en ny grænse inden for hetero -
 Mere bæredygtig genanvendelse af plastMobiltelefonetui lavet med 3D-print, ved brug af genbrugsplast. Kredit:Copyright:AG Mecking, Universitetet i Konstanz Plast er blandt de mest brugte materialer, og de er vitale komponenter i alle
Mere bæredygtig genanvendelse af plastMobiltelefonetui lavet med 3D-print, ved brug af genbrugsplast. Kredit:Copyright:AG Mecking, Universitetet i Konstanz Plast er blandt de mest brugte materialer, og de er vitale komponenter i alle
- Lørdagscitater:At lytte til fugledrømme, sikre qubits, forestille sig umuligt billard
- Nanopartikler, der bærer tre eller flere lægemidler, rummer potentiale for målrettet kræftbehand…
- Hvad er valenselektronkonfiguration for arsenatomet?
- Sådan forbedres din præcision i Lab
- Hvorfor produceres der vand, når brint forbrændes?
- Hvorfor er det så svært for mennesker at få en baby?


