Kovalent binding, hvor elektroner deles lige?
Her er hvorfor:
* Polaritet: Polaritet i et molekyle stammer fra en ujævn fordeling af elektroner.
* Lige deling: I en ikke -polær kovalent binding har de to involverede atomer lignende elektronegativitet. Elektronegativitet er et atoms evne til at tiltrække elektroner i en binding. Fordi atomerne har lignende elektronegativiteter, trækker de på de delte elektroner med lige kraft, hvilket resulterer i en jævn fordeling.
* Eksempel: Bindingen mellem to hydrogenatomer (H-H) i et brintmolekyle (H₂) er et klassisk eksempel på en ikke-polær kovalent binding.
Fortæl mig, hvis du gerne vil have flere eksempler eller vil udforske begrebet polære kovalente obligationer!
Sidste artikelI citronsyrecyklussen produceres ATP -molekyler af?
Næste artikelHvordan opdeles vandmolekyler fra hinanden?
 Varme artikler
Varme artikler
-
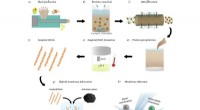 Dekontaminering af tungmetalvand ved hjælp af protein fra planteaffaldSkematisk over procesflow fra plantefrø til den amyloidbaserede filtreringsmembran. a) Fremstilling af solsikke- og jordnøddemel ved skruepresning af frø. b) Vandig proteinekstraktion af måltider (bru
Dekontaminering af tungmetalvand ved hjælp af protein fra planteaffaldSkematisk over procesflow fra plantefrø til den amyloidbaserede filtreringsmembran. a) Fremstilling af solsikke- og jordnøddemel ved skruepresning af frø. b) Vandig proteinekstraktion af måltider (bru -
 Forskere opfinder små, genlukkelige pakker til levering af materialer i køDenne simulering viser lagene i pakkerne - et sort ydre lag, en rød, udskifteligt lag, der forbinder de to, og det glasagtige inderlag i guld. Blå vandmolekyler omgiver pakken. Kredit:Lucas Antony
Forskere opfinder små, genlukkelige pakker til levering af materialer i køDenne simulering viser lagene i pakkerne - et sort ydre lag, en rød, udskifteligt lag, der forbinder de to, og det glasagtige inderlag i guld. Blå vandmolekyler omgiver pakken. Kredit:Lucas Antony -
 Producerer grønt brint ved udsættelse af nanomaterialer for sollysSe gennem et vindue af det indre af en ultrahøj vakuumreaktor, hvor TiO2-nanorør er dekoreret med CoO-nanopartikler. Vi ser flammen (plasma produceret ved laserablation), der sprutter CoOet for at giv
Producerer grønt brint ved udsættelse af nanomaterialer for sollysSe gennem et vindue af det indre af en ultrahøj vakuumreaktor, hvor TiO2-nanorør er dekoreret med CoO-nanopartikler. Vi ser flammen (plasma produceret ved laserablation), der sprutter CoOet for at giv -
 Video:Vil det kombucha?Kredit:The American Chemical Society Kombucha er en boblende, fermenteret te, der har vundet popularitet i sundheds- og wellness-scenen i løbet af det sidste årti – men hvad er det helt præcist?
Video:Vil det kombucha?Kredit:The American Chemical Society Kombucha er en boblende, fermenteret te, der har vundet popularitet i sundheds- og wellness-scenen i løbet af det sidste årti – men hvad er det helt præcist?
- Proces, der gør det muligt for celler at frigive energi anaerobt?
- Små kolber fremskynder kemiske reaktioner
- Hvilket enzym findes i spyt, og hvilken madtype virker det på?
- Forskere finder ud af, at nedkøling eller lufttørring af jordprøver til fremtidige undersøgelser…
- Tilfældet med de uklare filtre:Løsning af mysteriet med de nedværdigende sollysdetektorer
- Grøn zone:Efter to år, betalte alle hendes miljøvenlige projekter sig?


