Olie og vand:Forstå hvorfor de ikke blandes - en videnskabelig forklaring
* Polaritet: Vandmolekyler er polære , hvilket betyder, at de har en lidt positiv ende og en lidt negativ ende på grund af den ujævne deling af elektroner. Dette skaber en stærk tiltrækning mellem vandmolekyler og danner brintbindinger.
* Ikke-polaritet: Oliemolekyler er på den anden side ikke-polære . Deres elektroner deles mere jævnt, hvilket resulterer i ingen signifikante positive eller negative ladninger.
Hvorfor er det vigtigt:
* Like opløses som: Polære stoffer har en tendens til at opløse andre polære stoffer, mens ikke-polære stoffer opløser andre ikke-polære stoffer.
* Ublandbarhed: Vand, der er polært, har ikke en stærk tiltrækning til de ikke-polære oliemolekyler. I stedet for at opløses adskilles de to stoffer, hvor olien flyder ovenpå, fordi den er mindre tæt.
Tænk på det på denne måde: Forestil dig at prøve at blande magneter med ikke-magnetiske genstande. Magneterne ville klæbe sammen og danne separate klumper, mens de ikke-magnetiske objekter ville forblive adskilte.
Det samme princip gælder for olie og vand. Den stærke tiltrækning mellem vandmolekyler forhindrer dem i at blande sig med olie, hvilket skaber to adskilte lag.
 Varme artikler
Varme artikler
-
 En enklere model kommer til sagen med proteinerCecilia Clementi. Kredit:Jeff Fitlow/Rice University Beregningsmodeller er kommet langt i deres evne til at simulere de mest basale biologiske processer, såsom hvordan proteiner folder. En ny tekn
En enklere model kommer til sagen med proteinerCecilia Clementi. Kredit:Jeff Fitlow/Rice University Beregningsmodeller er kommet langt i deres evne til at simulere de mest basale biologiske processer, såsom hvordan proteiner folder. En ny tekn -
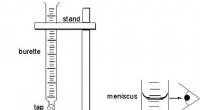 Direkte titrering:Præcis kvantificering af opløste stoffer i opløsningAf Chuck Robert | Opdateret 30. august 2022 Direkte titrering er den analytiske arbejdshest til at bestemme den nøjagtige mængde af et ukendt opløst stof i en opløsning. Ved omhyggeligt at tilføje en
Direkte titrering:Præcis kvantificering af opløste stoffer i opløsningAf Chuck Robert | Opdateret 30. august 2022 Direkte titrering er den analytiske arbejdshest til at bestemme den nøjagtige mængde af et ukendt opløst stof i en opløsning. Ved omhyggeligt at tilføje en -
 Ny indsigt i rotavirusmekanik kan føre til forbedrede behandlingerKunstnerisk gengivelse af rotaviruspartikeldissektionsprocessen, udført med atomkraftmikroskopi. Kredit:Billede skabt af Scixel (scixel.es/), under instruktionerne af D. Luque og P. J. de Pablo. F
Ny indsigt i rotavirusmekanik kan føre til forbedrede behandlingerKunstnerisk gengivelse af rotaviruspartikeldissektionsprocessen, udført med atomkraftmikroskopi. Kredit:Billede skabt af Scixel (scixel.es/), under instruktionerne af D. Luque og P. J. de Pablo. F -
 Genomminedrift afslører ny produktionsvej til lovende malariabehandlingElizabeth Parkinson, venstre, Lektor i kemi, Purdue University med G. William Arends Professor i molekylær og cellulær biologi William Metcalf, ret. Kredit:University of Illinois at Urbana-Champaign
Genomminedrift afslører ny produktionsvej til lovende malariabehandlingElizabeth Parkinson, venstre, Lektor i kemi, Purdue University med G. William Arends Professor i molekylær og cellulær biologi William Metcalf, ret. Kredit:University of Illinois at Urbana-Champaign
- Hvordan lander raketten på jorden?
- En række processer på overfladen og i skorpemantelen, der langsomt skifter klipper fra en slags ti…
- Sådan ved du, hvornår det er sikkert, klik på 'afmeld' på spam-mail
- Kobber nanotråde kan blive grundlaget for nye solceller
- Sådan beregnes koncentrationen i en titrering:Trin-for-trin-vejledning
- Hvor er Peridot udvindet, og hvordan?


