Vand:Det universelle opløsningsmiddel - Forståelse af kemisk opløsning
Her er hvorfor:
* Polaritet: Vandmolekyler har en positiv og negativ ende på grund af den ujævne deling af elektroner. Denne polaritet gør det muligt for vand at tiltrække og omgive andre polære molekyler, bryder dem fra hinanden og opløser dem.
* Brintbinding: Vandmolekyler danner stærke hydrogenbindinger med hinanden og med andre polære molekyler, hvilket yderligere hjælper i opløsningsprocessen.
* Høj dielektrisk konstant: Vands høje dielektriske konstant svækker de elektrostatiske kræfter mellem ioner, hvilket gør det lettere for dem at adskille og opløses.
Mens vand er det mest almindelige opløsningsmiddel, er andre opløsningsmidler såsom alkoholer og acetone også have evnen til at opløse visse stoffer. Vands unikke egenskaber gør det dog til det vigtigste og mest alsidige opløsningsmiddel til en lang række kemikalier.
 Varme artikler
Varme artikler
-
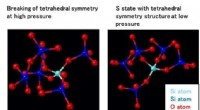 Strukturel oprindelse af de unormale egenskaber af SiO2-glas under trykStrukturelle træk ved SiO2-glas under tryk. / Translationel rækkefølge i SiO2-glas som funktion af parameteren z opnået i vores eksperiment med MD-RMC-modellering og MD-simulering med BKS-model ved 0
Strukturel oprindelse af de unormale egenskaber af SiO2-glas under trykStrukturelle træk ved SiO2-glas under tryk. / Translationel rækkefølge i SiO2-glas som funktion af parameteren z opnået i vores eksperiment med MD-RMC-modellering og MD-simulering med BKS-model ved 0 -
 Elektrodeposition og udglødning bruges til at muliggøre justering af hårdhed i nanokornede metall…Mikrostruktur af den aflejrede nanokornede Ni-Mo-legering. (A) Bright-field og (B) dark-field billeder af den afsatte Ni-21,5% Mo prøve. (Indsæt) Et tilsvarende valgt områdediffraktionsmønster. (C) Et
Elektrodeposition og udglødning bruges til at muliggøre justering af hårdhed i nanokornede metall…Mikrostruktur af den aflejrede nanokornede Ni-Mo-legering. (A) Bright-field og (B) dark-field billeder af den afsatte Ni-21,5% Mo prøve. (Indsæt) Et tilsvarende valgt områdediffraktionsmønster. (C) Et -
 Rumtemperaturbundet grænseflade forbedrer afkøling af galliumnitrid-enhederTværsnit af lysfelt højopløsnings STEM-billeder af GaN-diamant-grænseflader bundet ved overfladeaktiveret bindingsteknik. Kredit:Zhe Cheng, Georgia Tech En rumtemperaturbindingsteknik til at integ
Rumtemperaturbundet grænseflade forbedrer afkøling af galliumnitrid-enhederTværsnit af lysfelt højopløsnings STEM-billeder af GaN-diamant-grænseflader bundet ved overfladeaktiveret bindingsteknik. Kredit:Zhe Cheng, Georgia Tech En rumtemperaturbindingsteknik til at integ -
 Nyt madfrysningskoncept forbedrer kvaliteten, øger sikkerheden, reducerer energiforbrugetKredit:Unsplash/CC0 Public Domain Skift til en ny madfrysningsmetode kunne give sikrere og bedre kvalitet frosne fødevarer, samtidig med at der spares energi og reduceres kulstofemissioner, ifølge
Nyt madfrysningskoncept forbedrer kvaliteten, øger sikkerheden, reducerer energiforbrugetKredit:Unsplash/CC0 Public Domain Skift til en ny madfrysningsmetode kunne give sikrere og bedre kvalitet frosne fødevarer, samtidig med at der spares energi og reduceres kulstofemissioner, ifølge
- Almindelige edderkopper i det sydlige Texas
- Crawler sociale medier for at forstå den ulovlige motorcykelbande-dynamik
- Hvilken er også aftenstjernen har en på 500 grader celsius og skyer svovlsyre?
- Finansiering skal stilles til rådighed for grønne iværksættere for at sikre et netto-nul CO2-udl…
- Eksempler på vindpollinerede blomster
- Forståelse af opløsning:Hvordan faste stoffer spredes i væsker


