Forståelse af vands tiltrækning til natriumchlorid (salt)
* Polaritet: Vandmolekyler er polære, hvilket betyder, at de har en positiv og negativ ende på grund af den ujævne fordeling af elektroner. Iltatomet er svagt negativt, mens brintatomerne er svagt positive.
* Ionisk binding: Natriumchlorid er en ionisk forbindelse. Det betyder, at det er dannet af den elektrostatiske tiltrækning mellem positivt ladede natriumioner (Na+) og negativt ladede chloridioner (Cl-).
* Attraktion: De positive ender af vandmolekyler tiltrækkes af de negativt ladede chloridioner, mens de negative ender af vandmolekyler tiltrækkes af de positivt ladede natriumioner. Denne attraktion kaldes elektrostatisk tiltrækning .
* Hydration Shell: Vandmolekyler omgiver ionerne og danner en hydreringsskal. Denne skal isolerer effektivt ionerne fra hinanden, svækker ionbindingerne og tillader saltet at opløses i vand.
Kort sagt gør den polære natur af vandmolekyler det muligt for dem at interagere med de ladede ioner af natriumchlorid, hvorved de effektivt trækker dem fra hinanden og opløser saltet.
Her er nogle yderligere punkter:
* Energi: Processen med at opløse salt i vand er en endoterm proces , hvilket betyder, at det kræver energi. Denne energi kommer fra brydningen af ionbindingerne i saltkrystallen og dannelsen af nye bindinger mellem vandmolekyler og ioner.
* Opløselighed: Opløseligheden af natriumchlorid i vand er relativt høj, hvilket betyder, at en stor mængde salt kan opløses i en given mængde vand. Dette skyldes den stærke tiltrækning mellem vandmolekyler og ionerne.
Samlet set er tiltrækningen mellem vandmolekyler og natriumchlorid en nøglefaktor i opløsningen af salt i vand, en proces, der er afgørende for mange biologiske og kemiske processer.
 Varme artikler
Varme artikler
-
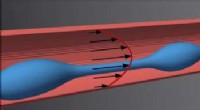 Fysikere opdager mekanismer til dannelse af blodpladerIndividuelle dråber dannes af en aflang fingerformet celle (blå) i blodgennemstrømningen. Hver dråbe udvikler sig til en blodplade. Billede:UBT / Christian Bächer. Kredit:University of Bayreuth Bl
Fysikere opdager mekanismer til dannelse af blodpladerIndividuelle dråber dannes af en aflang fingerformet celle (blå) i blodgennemstrømningen. Hver dråbe udvikler sig til en blodplade. Billede:UBT / Christian Bächer. Kredit:University of Bayreuth Bl -
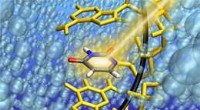 RNA-strengen muliggør indfangning af uracil i den kritiske tilstandKredit:Ludwig Maximilian Universitetet i München Forskere ledet af Regina de Vivie-Riedle, professor i teoretisk kemi ved LMU München, har fundet indikationer for en base-uafhængig mekanisme, der
RNA-strengen muliggør indfangning af uracil i den kritiske tilstandKredit:Ludwig Maximilian Universitetet i München Forskere ledet af Regina de Vivie-Riedle, professor i teoretisk kemi ved LMU München, har fundet indikationer for en base-uafhængig mekanisme, der -
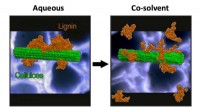 Supercomputing forbedrer biomassebrændstofkonverteringCo-opløsningsmidler THF og vand får lignin til at adskille sig fra sig selv og cellulose, udvides til en tilfældig spole. Kredit:Charles Cai/UCR Brændstoffer fremstillet af landbrugs- eller skovbr
Supercomputing forbedrer biomassebrændstofkonverteringCo-opløsningsmidler THF og vand får lignin til at adskille sig fra sig selv og cellulose, udvides til en tilfældig spole. Kredit:Charles Cai/UCR Brændstoffer fremstillet af landbrugs- eller skovbr -
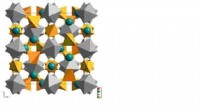 Oprettelse af et nyt kompositbrændstof til næste generations hurtige reaktorerKrystalstrukturen af yttrium-aluminium granat. Kredit:Lobachevsky University Fælles forskningsindsats af et team af videnskabsmænd ved Lobachevsky University of Nizhny Novgorod (UNN), bestående
Oprettelse af et nyt kompositbrændstof til næste generations hurtige reaktorerKrystalstrukturen af yttrium-aluminium granat. Kredit:Lobachevsky University Fælles forskningsindsats af et team af videnskabsmænd ved Lobachevsky University of Nizhny Novgorod (UNN), bestående
- Er det sandt eller falsk, at overførsel af termisk energi ved stråling ikke kræver stof?
- Fejl på fabrikken i Seattle dumper millioner af gallons spildevand
- Hvorfor er skorpen svær at bore ind i?
- Teknikken karakteriserer faser af superfluider, der skifter til supersolider og tilbage
- Hvad er miljøet, der er nødvendigt for kul til at danne sig?
- Angiver ændringer i hastighed på et objekt altid en hastighed?


