Syre-base neutralisering:Forstå reaktionen
Her er en opdeling:
* Syrer indeholder hydrogenioner (H+) og har en pH mindre end 7.
* Alkalier indeholder hydroxidioner (OH-) og har en pH-værdi på over 7.
* Når de blandes, reagerer hydrogenionerne fra syren med hydroxidionerne fra alkaliet og danner vand (H2O).
* De resterende ioner fra syre og alkali kombineres for at danne et salt.
Her er et simpelt eksempel:
Saltsyre (HCl) + Natriumhydroxid (NaOH) → Natriumchlorid (NaCl) + Vand (H2O)
* HCl er en syre, der giver H+ ioner.
* NaOH er et alkali, der giver OH-ioner.
* NaCl er det dannede salt (bordsalt).
Nøglepunkter:
* Reaktionen er exoterm , hvilket betyder, at der frigives varme.
* pH-værdien af den resulterende opløsning vil være tættere på neutral (pH 7) end den oprindelige syre eller alkali.
* Den type salt, der dannes, afhænger af den specifikke syre og alkali, der anvendes.
Bemærk: Neutraliseringsreaktioner er vigtige på mange områder, herunder:
* Kemi: Afbalancering af pH-niveauer i opløsninger.
* Biologi: Vedligeholdelse af pH-balancen i vores kroppe.
* Branche: Produktion af forskellige kemikalier og materialer.
Sidste artikelSyre-syre-reaktioner:Forståelse af kemisk adfærd
Næste artikelSyre-basereaktioner:Forståelse af salte og vanddannelse
 Varme artikler
Varme artikler
-
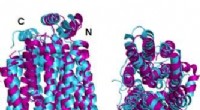 Ny forskning transformerer glukosetransportproteiner til vandopløselig formTo vinkler af den krystallinske struktur GLUT1 (magenta) glucosetransporterprotein overlejret med den AlphaFold2 computerforudsagte vandopløselige variant af det samme protein (cyan) viser, at det kry
Ny forskning transformerer glukosetransportproteiner til vandopløselig formTo vinkler af den krystallinske struktur GLUT1 (magenta) glucosetransporterprotein overlejret med den AlphaFold2 computerforudsagte vandopløselige variant af det samme protein (cyan) viser, at det kry -
 Elektrokemisk syntese af formiat fra kuldioxid ved anvendelse af en tin/reduceret grafenoxidkatalysa…Scanning elektronmikroskop billede (øverst til venstre), transmissionselektronmikroskopbillede (øverst til højre), reduktionskarakteristika (nederst til venstre) og Faradic -effektivitet (nederst til
Elektrokemisk syntese af formiat fra kuldioxid ved anvendelse af en tin/reduceret grafenoxidkatalysa…Scanning elektronmikroskop billede (øverst til venstre), transmissionselektronmikroskopbillede (øverst til højre), reduktionskarakteristika (nederst til venstre) og Faradic -effektivitet (nederst til -
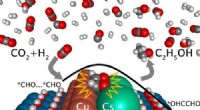 Katalysatorundersøgelse fremmer omdannelsen af kuldioxid til ethanolGrafisk abstrakt. Kredit:DOI:10.1021/jacs.1c03940 Et internationalt samarbejde mellem forskere har taget et væsentligt skridt hen imod realiseringen af en næsten grøn nul-net-kulstofteknologi, d
Katalysatorundersøgelse fremmer omdannelsen af kuldioxid til ethanolGrafisk abstrakt. Kredit:DOI:10.1021/jacs.1c03940 Et internationalt samarbejde mellem forskere har taget et væsentligt skridt hen imod realiseringen af en næsten grøn nul-net-kulstofteknologi, d -
 En grundlæggende mangel i luftforureningsmodellerKredit:CC0 Public Domain Forskere fra Københavns Universitet har opdaget et overraskende fænomen i en proces, hvorved visse gasmolekyler producerer skadelige partikler. Virkningen af dette fænom
En grundlæggende mangel i luftforureningsmodellerKredit:CC0 Public Domain Forskere fra Københavns Universitet har opdaget et overraskende fænomen i en proces, hvorved visse gasmolekyler producerer skadelige partikler. Virkningen af dette fænom
- Hvorfor bruges natrium som kølemiddel til atomreaktorer?
- Undersøgelse:Millennials arresteret oftere end forgængere - selv når der begås færre forbrydels…
- Hvad er betydningen af Jorden i romersk mytologi?
- Hvad er en glat forbindelse?
- Antal elektroner i kulstof:En simpel forklaring
- Fænotype:Definition, typer og eksempler


