Forståelse af metalstabilitet:Fortolkning af aktivitetsserien
Aktivitetsserie:
* Aktivitetsserien er en liste over metaller arrangeret i rækkefølge efter deres faldende reaktivitet.
* Metaller højere i serien er mere reaktive, hvilket betyder, at de let taber elektroner og danner kationer.
* Metaller lavere på serien er mindre reaktive, hvilket betyder, at de er mindre tilbøjelige til at miste elektroner og danne kationer.
Stabilitet:
* Stabile metaller er dem, der er mindre reaktive og modstår oxidation (tab af elektroner). De findes lettere i deres elementære tilstand.
* Ustabile metaller er dem, der er mere reaktive og let oxideres. De har tendens til at danne forbindelser med andre grundstoffer.
Sådan afspejler aktivitetsserien stabilitet:
* Metaller i toppen af serien (f.eks. lithium, kalium) er meget reaktive og oxideres let. De er ustabile i deres grundstofform og findes ofte i forbindelser.
* Metaller i bunden af serien (f.eks. guld, platin) er meget ureaktive og modstår oxidation. De er meget stabile i deres elementære form, hvilket gør dem velegnede til smykker og andre anvendelser, hvor modstand mod korrosion er vigtig.
Eksempel:
Overvej reaktionen mellem et metal og en syre.
* Et meget reaktivt metal (som kalium) vil let reagere med en syre, frigive brintgas og danne et salt. Dette indikerer, at kalium er ustabilt i sin elementære form og let danner en forbindelse.
* Et mindre reaktivt metal (som guld) vil ikke reagere med en syre. Dette viser guldets stabilitet i sin elementære form.
Konklusion:
Aktivitetsrækken af metaller afspejler direkte metallernes stabilitet. Metaller højere på serien er mindre stabile og mere reaktive, mens metaller lavere på serien er mere stabile og mindre reaktive. Denne forståelse hjælper med at forudsige metallers reaktivitet i forskellige kemiske reaktioner og deres egnethed til forskellige anvendelser.
 Varme artikler
Varme artikler
-
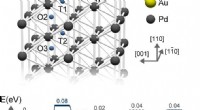 Hvorfor guld-palladium-legeringer er bedre end palladium til brintlagringAu-atomerne destabiliserer kemisorberet brint, dermed øge deres energi og reducere barrieren. Kredit:2018 Shohei Ogura, Institut for Industrividenskab, Universitetet i Tokyo Materialer, der absorb
Hvorfor guld-palladium-legeringer er bedre end palladium til brintlagringAu-atomerne destabiliserer kemisorberet brint, dermed øge deres energi og reducere barrieren. Kredit:2018 Shohei Ogura, Institut for Industrividenskab, Universitetet i Tokyo Materialer, der absorb -
 Fordelen ved 2D metal-organiske ramme-nanoark i sanseapplikationerGrafisk abstrakt. Kredit:LI Xixuan I de seneste år, fluorescerende metal-organiske rammer (MOFer) er blevet demonstreret som en lovende strategi til konstruktion af sensorer. Imidlertid, de fleste
Fordelen ved 2D metal-organiske ramme-nanoark i sanseapplikationerGrafisk abstrakt. Kredit:LI Xixuan I de seneste år, fluorescerende metal-organiske rammer (MOFer) er blevet demonstreret som en lovende strategi til konstruktion af sensorer. Imidlertid, de fleste -
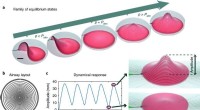 Ved at kombinere pneumatik med en hydrogel for at skabe en baromorf - til blød robotteknologien, Kontinuerlig familie af ligevægtstilstande opnået for en baromorf under forskellige tryk. b, Tilsvarende netværk af kanaler indlejret i pladen. Kanaler er mere koncentrerede i den centrale region
Ved at kombinere pneumatik med en hydrogel for at skabe en baromorf - til blød robotteknologien, Kontinuerlig familie af ligevægtstilstande opnået for en baromorf under forskellige tryk. b, Tilsvarende netværk af kanaler indlejret i pladen. Kanaler er mere koncentrerede i den centrale region -
 Ny teknologi til fremstilling af porøst aluminiumDen nye teknologi til fremstilling af usænkeligt materiale fra aluminiumslegeringen blev patenteret ved Peter the Great St. Petersburg Polytechnic University (SPbPU). Kredit:Peter den Store St. Peters
Ny teknologi til fremstilling af porøst aluminiumDen nye teknologi til fremstilling af usænkeligt materiale fra aluminiumslegeringen blev patenteret ved Peter the Great St. Petersburg Polytechnic University (SPbPU). Kredit:Peter den Store St. Peters


