Forståelse af formelenheder:Repræsenterer kemiske forbindelser
* Viser det enkleste hele talforhold mellem atomer af hvert grundstof, der er til stede i forbindelsen. Dette forhold definerer forbindelsens specifikke kemiske sammensætning. For eksempel har vand (H2O) altid to hydrogenatomer for hvert oxygenatom, uanset størrelsen af vandprøven.
* Giver en kortfattet og utvetydig repræsentation af forbindelsen. Det er en kortfattet måde at beskrive molekylet eller ionstrukturen på, hvilket gør det lettere at kommunikere og forstå kemisk information.
* Letter beregninger. Formelenheden giver os mulighed for at bestemme forbindelsens molekylvægt, molmasse og andre vigtige egenskaber.
Lad os se på nogle eksempler:
* Natriumchlorid (NaCl): Formlenheden angiver, at der er et natriumatom (Na) for hvert chloratom (Cl) i denne ioniske forbindelse.
* Glucose (C₆H₁2O6): Denne formelenhed viser, at hvert glucosemolekyle indeholder 6 carbonatomer, 12 hydrogenatomer og 6 oxygenatomer.
Sammenfattende giver formelenheden en grundlæggende repræsentation af en forbindelse, der giver os mulighed for at forstå dens sammensætning og egenskaber på en enkel og ensartet måde.
 Varme artikler
Varme artikler
-
 Nyt avanceret materiale viser ekstraordinær stabilitet over et bredt temperaturområdeForskere fra UNSW har fundet et ekstraordinært materiale, der ikke udvider sig eller trækker sig sammen over et ekstremt bredt temperaturområde og kan være et af de mest stabile materialer, man kender
Nyt avanceret materiale viser ekstraordinær stabilitet over et bredt temperaturområdeForskere fra UNSW har fundet et ekstraordinært materiale, der ikke udvider sig eller trækker sig sammen over et ekstremt bredt temperaturområde og kan være et af de mest stabile materialer, man kender -
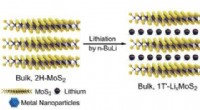 Brintproduktion i et begrænset rumFigur 1:Indkapslingen af ædelmetal nanopartikler i MoS2 ved en in-situ reduktion strategi. National University of Singapore kemikere har udviklet en metode til at begrænse ædelmetal -nanopartikl
Brintproduktion i et begrænset rumFigur 1:Indkapslingen af ædelmetal nanopartikler i MoS2 ved en in-situ reduktion strategi. National University of Singapore kemikere har udviklet en metode til at begrænse ædelmetal -nanopartikl -
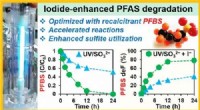 PFAS-kemikalier holder ikke evigtGrafisk abstrakt. Kredit:Environmental Science &Technology (2022). DOI:10.1021/acs.est.1c07608 Når de først er blevet kaldt kemikalier for evigt, kan per- og polyfluoralkyl-stoffer eller PFAS være
PFAS-kemikalier holder ikke evigtGrafisk abstrakt. Kredit:Environmental Science &Technology (2022). DOI:10.1021/acs.est.1c07608 Når de først er blevet kaldt kemikalier for evigt, kan per- og polyfluoralkyl-stoffer eller PFAS være -
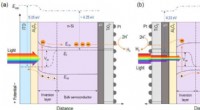 Rumlig afkobling af lysabsorption og reaktionssteder i n-Si fotokatoder til solvandssplitningSkematisk energibåndsdiagram over (a) belysningsreaktion afkoblet n-Si MIS fotokatode og (b) traditionel p-Si MIS fotokatode for HER under belysning. Kredit:Science China Press Solar-drevet fotoel
Rumlig afkobling af lysabsorption og reaktionssteder i n-Si fotokatoder til solvandssplitningSkematisk energibåndsdiagram over (a) belysningsreaktion afkoblet n-Si MIS fotokatode og (b) traditionel p-Si MIS fotokatode for HER under belysning. Kredit:Science China Press Solar-drevet fotoel
- Log-periodiske kvanteoscillationer og diskret skala-invariance i Dirac-materialer
- Kan tarmbakterier blive den næste sportsdrink?
- Afdækning af Temperance Betydning Tarot-kort
- Hvad er de cellulære organeller, der udfører respiration for at producere energi til celle?
- En farverig detektor
- Hvilke rocktyper vil være i alluviale fans?


