Natriumchloridopløsning:Forståelse af ioniske interaktioner i vand
* Ionbinding i NaCl: Natriumchlorid er en ionisk forbindelse. Det betyder, at det danner et krystalgitter, hvor natriumioner (Na+) og chloridioner (Cl-) holdes sammen af elektrostatisk tiltrækning.
* Opløsning i vand: Når NaCl opløses i vand, omgiver vandmolekylerne ionerne. Den positive ende af vandmolekylet (brintatomerne) tiltrækkes af de negative chloridioner, og den negative ende af vandmolekylet (iltatomet) tiltrækkes af de positive natriumioner. Denne proces kaldes hydrering .
* Ingen direkte obligationer: Mens vandmolekylerne er stærkt tiltrukket af ionerne, danner de ikke direkte kovalente bindinger med dem. I stedet er der ion-dipol-interaktioner . Disse er svagere end kovalente bindinger, men stadig stærke nok til at overvinde de ioniske kræfter, der holder NaCl-krystallen sammen.
Derfor er der ikke 4 bindinger, men derimod mange ion-dipol-interaktioner mellem vandmolekyler og natrium- og chloridionerne, når NaCl opløses i vand.
 Varme artikler
Varme artikler
-
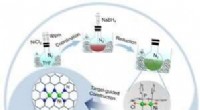 Forskere designer dinuclear-site katalysatorer og afslører den underliggende mekanismeSynteseskema. Kredit:DING Tao et al. Dinuclear-site katalysatorer (DSCer) har tiltrukket sig mere og mere opmærksomhed fra forskere på grund af deres fremragende katalytiske evne ved at inkorporer
Forskere designer dinuclear-site katalysatorer og afslører den underliggende mekanismeSynteseskema. Kredit:DING Tao et al. Dinuclear-site katalysatorer (DSCer) har tiltrukket sig mere og mere opmærksomhed fra forskere på grund af deres fremragende katalytiske evne ved at inkorporer -
 Udnyttelse af kropsvarmen til at drive elektroniske enhederUdviklingen af effektive termoelektriske materialer betyder, at kropsvarme alene fra, sige, en persons hånd, kan bruges til at drive små bærbare enheder, i dette tilfælde en rød LED. Kredit:A*STAR I
Udnyttelse af kropsvarmen til at drive elektroniske enhederUdviklingen af effektive termoelektriske materialer betyder, at kropsvarme alene fra, sige, en persons hånd, kan bruges til at drive små bærbare enheder, i dette tilfælde en rød LED. Kredit:A*STAR I -
 Elektrokemisk iltudvikling på Hf2B2Ir5 elektrodematerialeOER ydeevne af Hf2B2Ir5 anode materiale, repræsenteret ved lineære sweep voltammogrammer målt under det langsigtede kronopotentiometrieksperiment (0,1 M H2SO4, j =100 mA cm-2, t =0 ... 240 h). Indsat:
Elektrokemisk iltudvikling på Hf2B2Ir5 elektrodematerialeOER ydeevne af Hf2B2Ir5 anode materiale, repræsenteret ved lineære sweep voltammogrammer målt under det langsigtede kronopotentiometrieksperiment (0,1 M H2SO4, j =100 mA cm-2, t =0 ... 240 h). Indsat: -
 Ny klasse af solceller, brug af blyfri perovskitmaterialerBlyfri Perovskite flim (til venstre) og farvefølsomme organiske solceller (højre). Kredit:UNIST Blybaserede perovskiter er lovende materialer til billige og højeffektive solceller. Imidlertid, den
Ny klasse af solceller, brug af blyfri perovskitmaterialerBlyfri Perovskite flim (til venstre) og farvefølsomme organiske solceller (højre). Kredit:UNIST Blybaserede perovskiter er lovende materialer til billige og højeffektive solceller. Imidlertid, den
- E3 videospilskonference aflyst på grund af coronavirus
- Hvordan er forholdet mellem frekvens og bølgelængde af elektromagnetisk energi?
- At undervise AI-agenter i at navigere underrutiner ved at give dem videoer
- Forskere indser lydløs foton-ekko-protokol
- Hvad er strukturformlen for natriumstearat en type sæbe?
- Effekten af vandforurening på planter og dyr


