Polaritet af NCl3-bindinger:Forståelse af kemiske bindinger
* Elektronegativitet: Nitrogen (N) har en elektronegativitet på 3,04, mens klor (Cl) har en elektronegativitet på 3,16. Denne forskel i elektronegativitet, selvom den er lille, skaber et dipolmoment inden for hver N-Cl-binding.
* Dipolmoment: Kloratomet tiltrækker de delte elektroner i bindingen stærkere end nitrogenatomet. Dette skaber en delvis negativ ladning (δ-) på chloratomet og en delvis positiv ladning (δ+) på nitrogenatomet.
* Polær kovalent binding: På grund af den ujævne deling af elektroner og det resulterende dipolmoment, betragtes N-Cl-bindingerne i NCl3 som polære kovalente bindinger.
Vigtig bemærkning: Mens de individuelle bindinger i NCl3 er polære, er selve det samlede molekyle polært . Dette skyldes, at den molekylære geometri af NCl3 er trigonal pyramideformet, hvilket fører til et netto dipolmoment på tværs af molekylet.
 Varme artikler
Varme artikler
-
 Omdannelse af svovldioxid fra skadelig til nyttigKredit:CC0 Public Domain Forskere har skabt molekylære bure i en polymer for at fange skadelig svovldioxidforurening for at omdanne den til nyttige forbindelser og reducere affald og emissioner.
Omdannelse af svovldioxid fra skadelig til nyttigKredit:CC0 Public Domain Forskere har skabt molekylære bure i en polymer for at fange skadelig svovldioxidforurening for at omdanne den til nyttige forbindelser og reducere affald og emissioner. -
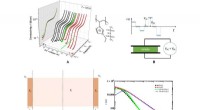 Kapacitans af tynde film indeholdende polymeriserede ioniske væskerDetaljer om bredbånds dielektrisk spektroskopi (BDS) målinger, kemisk struktur af PolyIL studeret i dette arbejde sammen med elektrodepolarisationsmodellen, der bruges til fortolkning af eksperimentel
Kapacitans af tynde film indeholdende polymeriserede ioniske væskerDetaljer om bredbånds dielektrisk spektroskopi (BDS) målinger, kemisk struktur af PolyIL studeret i dette arbejde sammen med elektrodepolarisationsmodellen, der bruges til fortolkning af eksperimentel -
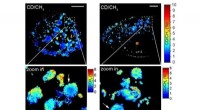 Forskere forstørrer skjulte biologiske strukturer ved at kombinere SRS og ekspansionsmikroskopiMAGNIFIERS fangede nyligt syntetiserede Huntingtin-aggregater (i rødt) med opløsning i nanoskala i Huntington-sygdomsmodellen. Kredit:Carnegie Mellon University Et forskerhold fra Carnegie Mellon U
Forskere forstørrer skjulte biologiske strukturer ved at kombinere SRS og ekspansionsmikroskopiMAGNIFIERS fangede nyligt syntetiserede Huntingtin-aggregater (i rødt) med opløsning i nanoskala i Huntington-sygdomsmodellen. Kredit:Carnegie Mellon University Et forskerhold fra Carnegie Mellon U -
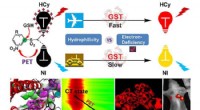 Fluorophores elektronmangel påvirker genkendelsesevnen af nær-infrarøde fluorescerende proberFluorophores elektronmangel kan påvirke genkendelsesydelsen af nær-infrarøde fluorescerende prober. Kredit:ZHANG Xuexiang Glutathion S-transferaser (GST) er et af de vigtigste fase II afgiftning
Fluorophores elektronmangel påvirker genkendelsesevnen af nær-infrarøde fluorescerende proberFluorophores elektronmangel kan påvirke genkendelsesydelsen af nær-infrarøde fluorescerende prober. Kredit:ZHANG Xuexiang Glutathion S-transferaser (GST) er et af de vigtigste fase II afgiftning


