Ledning:Hvorfor væsker og gasser er dårlige ledere (med undtagelser)
1. Partikelafstand:
* Fast: Atomer og molekyler i faste stoffer er tæt pakket, hvilket giver mulighed for let overførsel af ladning gennem et netværk af interagerende elektroner.
* Væsker og gasser: Partikler er mere spredt ud. I væsker, mens de er tættere på end i gasser, har de mere frihed til at bevæge sig rundt. Denne afstand gør det sværere for ladningsbærere (elektroner) at "hoppe" fra den ene partikel til den næste.
2. Gratis elektroner:
* Fast: Nogle faste stoffer, især metaller, har frie elektroner, der let kan bevæge sig gennem materialet. Disse elektroner fungerer som ladningsbærere, hvilket gør dem til fremragende ledere.
* Væsker og gasser: De fleste væsker og gasser har ikke et stort antal frie elektroner. I nogle tilfælde kan de have ioner, der kan bære ladning, men disse er normalt mindre mobile end frie elektroner.
Undtagelser:
* Elektrolytter: Nogle væsker, kaldet elektrolytter, er gode ledere, fordi de indeholder opløste ioner, der kan bevæge sig frit og føre elektrisk strøm. Eksempler omfatter saltvand, batterisyre og smeltede salte.
* Plasma: Gasser, der er blevet ioniseret (atomer har mistet eller fået elektroner) bliver stærkt ledende. Dette skyldes, at de frie elektroner og ioner i et plasma nemt kan bevæge sig og bære ladning.
Opsummering:
Mens mange væsker og gasser er dårlige ledere sammenlignet med faste stoffer, afhænger et materiales ledningsevne af dets specifikke sammensætning og egenskaber. Nogle væsker og gasser kan være fremragende ledere, især dem med frie ladningsbærere (elektroner eller ioner).
 Varme artikler
Varme artikler
-
 Forskere finder nye måder at bruge bioraffinaderikemikalier påSkræddersyede designerbakterier som fremtidige værktøjer i valoriseringen af bioraffinaderi-furaner. Kredit:Jan Deska Forskere fra gruppen Synthetic Organic Chemistry ved Aalto Universitet har e
Forskere finder nye måder at bruge bioraffinaderikemikalier påSkræddersyede designerbakterier som fremtidige værktøjer i valoriseringen af bioraffinaderi-furaner. Kredit:Jan Deska Forskere fra gruppen Synthetic Organic Chemistry ved Aalto Universitet har e -
 Udfordring forudsiger, hvordan metaller med komplekse former og fremstilling vil brydeMaterialeforsker Brad Boyce, arbejde med kolleger på Sandia National Laboratories, organiseret flere udfordringer for forskere, der arbejder på at forbedre forudsigelser for brud i duktile metaller. K
Udfordring forudsiger, hvordan metaller med komplekse former og fremstilling vil brydeMaterialeforsker Brad Boyce, arbejde med kolleger på Sandia National Laboratories, organiseret flere udfordringer for forskere, der arbejder på at forbedre forudsigelser for brud i duktile metaller. K -
 Hvor kommer denne forurening fra?Testresultater:To røde striber viser, at der er en forurening. Kredit:Vienna University of Technology Når vandområder bliver forurenet, det er vigtigt at finde årsagen så hurtigt og så økonomisk s
Hvor kommer denne forurening fra?Testresultater:To røde striber viser, at der er en forurening. Kredit:Vienna University of Technology Når vandområder bliver forurenet, det er vigtigt at finde årsagen så hurtigt og så økonomisk s -
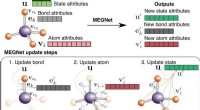 Ingeniører bruger grafnetværk til nøjagtigt at forudsige egenskaber af molekyler og krystallerSkematisk illustration af MEGNet-modeller. Kredit:Chi Chen/Materials Virtual Lab Nanoingeniører ved University of California San Diego har udviklet nye deep learning-modeller, der præcist kan foru
Ingeniører bruger grafnetværk til nøjagtigt at forudsige egenskaber af molekyler og krystallerSkematisk illustration af MEGNet-modeller. Kredit:Chi Chen/Materials Virtual Lab Nanoingeniører ved University of California San Diego har udviklet nye deep learning-modeller, der præcist kan foru
- Hvad er Jordens ydre mest fysiske lag opdelt i tektoniske plader?
- Molekyle angriber coronavirus på en ny måde
- Et objekt har været placeret kredset om solen i en afstand fra 65 AU Hvad er omtrentlig orbital per…
- Hvor mange protoner elektroner og neutroner har ox ygen?
- Indeholder en konstellation kun tilsluttede stjerner?
- Når natrium og chlorid sammenføjes, overføres et elektron fra den form en binding, hvad kaldes?


