Aluminium og nitrogenbinding:Ionisk vs. kovalent
* Elektronegativitetsforskel: Ionbindinger dannes typisk mellem grundstoffer med en stor elektronegativitetsforskel (større end 1,7). Aluminium har en elektronegativitet på 1,61, og nitrogen har en elektronegativitet på 3,04. Forskellen er 1,43, hvilket ikke er stort nok til at skabe en ægte ionbinding.
* Deling af elektroner: I stedet for at det ene element fuldstændigt overfører elektroner til det andet, deler aluminium og nitrogen elektroner for at opnå en stabil oktetkonfiguration. Denne deling af elektroner er karakteristisk for kovalent binding.
Opsummering: Mens aluminiumnitrid er en polær forbindelse (på grund af elektronegativitetsforskellen), betragtes det ikke som en ionisk forbindelse.
Sidste artikelpH af læsket kalk (Calciumhydroxid):Forstå alkalinitet
Næste artikelIlt- og nitrogenbinding:Ionisk vs. kovalent
 Varme artikler
Varme artikler
-
 Sådan tegner du et atoms atomstruktur:En trin-for-trin guideAf bidragyder – Opdateret 24. marts 2022 At tegne et atoms struktur er ligetil, når du først forstår dets grundlæggende komponenter:kernen, protoner, neutroner og elektronskaller. Denne guide fører d
Sådan tegner du et atoms atomstruktur:En trin-for-trin guideAf bidragyder – Opdateret 24. marts 2022 At tegne et atoms struktur er ligetil, når du først forstår dets grundlæggende komponenter:kernen, protoner, neutroner og elektronskaller. Denne guide fører d -
 Forbedret forståelse af industrielle elektrodeprocesserElektroden, der bruges til målingerne, er kun en hundrededel i tykkelsen af et menneskehår. Kredit:RUB, Marquard I den industrielle produktion af klor, specielle elektroder er for nylig blevet i
Forbedret forståelse af industrielle elektrodeprocesserElektroden, der bruges til målingerne, er kun en hundrededel i tykkelsen af et menneskehår. Kredit:RUB, Marquard I den industrielle produktion af klor, specielle elektroder er for nylig blevet i -
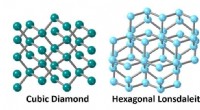 Vi skabte diamanter på få minutter uden varme ved at efterligne kraften ved en asteroide -kollisio…Krystalstrukturerne i kubisk diamant og sekskantet Lonsdaleite har atomer arrangeret forskelligt. I naturen, diamanter dannes dybt i jorden over milliarder af år. Denne proces kræver miljøer med u
Vi skabte diamanter på få minutter uden varme ved at efterligne kraften ved en asteroide -kollisio…Krystalstrukturerne i kubisk diamant og sekskantet Lonsdaleite har atomer arrangeret forskelligt. I naturen, diamanter dannes dybt i jorden over milliarder af år. Denne proces kræver miljøer med u -
 Forskere laver smartphone-system til at teste for bly i vandForskere byggede et selvstændigt smartphonemikroskop, der kan fungere i både fluorescens- og mørkfeltsbilledtilstande og parrede det med en billig Lumina 640-smartphone med et 8-megapixel kamera. Kred
Forskere laver smartphone-system til at teste for bly i vandForskere byggede et selvstændigt smartphonemikroskop, der kan fungere i både fluorescens- og mørkfeltsbilledtilstande og parrede det med en billig Lumina 640-smartphone med et 8-megapixel kamera. Kred


