Forståelse af ioniske bindinger:Dannelse, kationer og anioner
Ionbindinger dannes, når et metalatom mister en eller flere elektroner for at blive en positivt ladet kation, og et ikke-metalatom får disse elektroner til at blive en negativt ladet anion. De modsat ladede ioner tiltrækkes derefter af hinanden gennem elektrostatiske kræfter og danner en stærk ionbinding.
Her er en opdeling:
* Metaller har en tendens til at have lav ioniseringsenergi, hvilket betyder, at de let mister elektroner for at danne positive ioner (kationer).
* Ikke-metaller tendens til at have høje elektronaffiniteter, hvilket betyder, at de let får elektroner til at danne negative ioner (anioner).
* Tiltrækningen mellem de modsat ladede ioner kaldes en elektrostatisk kraft , som er meget stærk og resulterer i dannelsen af en stabil ionforbindelse.
Eksempel:
Natrium (Na), et metal, mister let en elektron for at blive Na⁺. Klor (Cl), et ikke-metal, får let en elektron til at blive Cl⁻. De modsat ladede ioner Na⁺ og Cl⁻ tiltrækker hinanden gennem elektrostatiske kræfter og danner den ioniske forbindelse natriumchlorid (NaCl), almindeligvis kendt som bordsalt.
Sidste artikelBeregning af atomer i en kemisk formel:3CaCl₂
Næste artikelBiologisk nedbrydeligt organisk affald:Hvad nedbryder naturligt?
 Varme artikler
Varme artikler
-
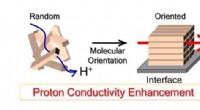 Få mere kontrol over brændselscellemembranerMolekylær orientering forbedrer protonkonduktion i protonkonduktive polymerer. Kredit:Yuki Nagao Mere organisering på molekylært niveau kan forbedre effektiviteten af membraner, der bruges i bri
Få mere kontrol over brændselscellemembranerMolekylær orientering forbedrer protonkonduktion i protonkonduktive polymerer. Kredit:Yuki Nagao Mere organisering på molekylært niveau kan forbedre effektiviteten af membraner, der bruges i bri -
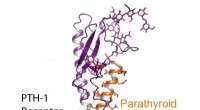 Fra receptorstruktur til nye osteoporoselægemidlerReceptoren er den vigtigste regulatoriske kontakt, der kontrollerer calciumfrigivelse fra knogler, og dermed et primært mål for udvikling af nye lægemidler til behandling af osteoporose. Receptoren be
Fra receptorstruktur til nye osteoporoselægemidlerReceptoren er den vigtigste regulatoriske kontakt, der kontrollerer calciumfrigivelse fra knogler, og dermed et primært mål for udvikling af nye lægemidler til behandling af osteoporose. Receptoren be -
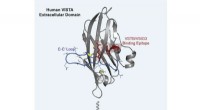 Ny indsigt i et kræftbeskyttende protein kan guide en ny generation af kræftbehandlingerVed hjælp af en kombination af beregning og eksperiment, forskere var i stand til at kortlægge formen på VISTA, et checkpoint protein, der forsvarer kræftceller mod immunsystemangreb, samt den del af
Ny indsigt i et kræftbeskyttende protein kan guide en ny generation af kræftbehandlingerVed hjælp af en kombination af beregning og eksperiment, forskere var i stand til at kortlægge formen på VISTA, et checkpoint protein, der forsvarer kræftceller mod immunsystemangreb, samt den del af -
 Vibration kun i én retningDet nydesignede materiale. Den transmitterer vibrationer fra venstre mod højre, men ikke fra højre mod venstre. Kredit:UvA/Brandenbourger et al. Elektroniske komponenter såsom transistorer transmi
Vibration kun i én retningDet nydesignede materiale. Den transmitterer vibrationer fra venstre mod højre, men ikke fra højre mod venstre. Kredit:UvA/Brandenbourger et al. Elektroniske komponenter såsom transistorer transmi
- Andromeda Galaxy i modsætning til de fleste andre galakser har?
- 12 af de ældste genstande, der nogensinde er opdaget
- MAVEN afslører, at Mars har metal i sin atmosfære
- Hvad er forskellen mellem sonometre og centimeter?
- Når temperaturen øger væskepartiklerne inde i et termometer begynder at bevæge sig hurtigere, og…
- Kan lysenergi absorberes på en overskyet dag?


