Syntesegas til metankonvertering:trykkets rolle
Reaktionen:
CO + 3H2 ⇌ CH4 + H2O
Le Chateliers princip:
Le Chateliers princip siger, at hvis en tilstandsændring anvendes på et system i ligevægt, vil systemet skifte i en retning, der aflaster stress. I dette tilfælde er stigende pres stressen.
Skift ligevægt:
Syntesegas til methan-reaktionen har 4 mol reaktanter (1 CO + 3 H2) og 2 mol produkter (1 CH4 + 1 H2O). Derfor vil en forøgelse af trykket favorisere den side med færre mol gas, som er produktsiden.
Konklusion:
Ved at øge trykket tvinger man ligevægten til at skifte mod dannelsen af metan og øger derved ligevægtsomdannelsen af syntesegas til metan.
Sidste artikelOxidationstal af Br₂:En klar forklaring
Næste artikelHomogene blandinger:definition, eksempler og karakteristika
 Varme artikler
Varme artikler
-
 Samtidig måling af biofysiske egenskaber og position af enkelte celler i en mikroenhedSkematisk design af den elektriske sensingregion i den mikrofluidiske impedanscytometrianordning. Den laterale position af enkelte partikler eller celler, der strømmer gennem de N-formede elektroder,
Samtidig måling af biofysiske egenskaber og position af enkelte celler i en mikroenhedSkematisk design af den elektriske sensingregion i den mikrofluidiske impedanscytometrianordning. Den laterale position af enkelte partikler eller celler, der strømmer gennem de N-formede elektroder, -
 Dyrkning af polymerer med forskellige længderSymbolsk repræsentation af, hvordan spredningen af et plastik kan kontrolleres ved at blande to katalysatorer (malerør). Kredit:Whitfield R et al, Chem, 2020 ETH-forskere har udviklet en ny meto
Dyrkning af polymerer med forskellige længderSymbolsk repræsentation af, hvordan spredningen af et plastik kan kontrolleres ved at blande to katalysatorer (malerør). Kredit:Whitfield R et al, Chem, 2020 ETH-forskere har udviklet en ny meto -
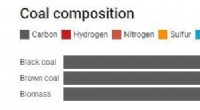 Hvordan laver vi brint af kul, og er det virkelig et rent brændstof?Kredit:Samtalen Energigiganten AGL afslørede i denne uge planer om at producere brintkraft på deres Loy Yang A-kulstation. Men hvordan forvandler vi kul, som ofte opfattes som blot lavet af kulsto
Hvordan laver vi brint af kul, og er det virkelig et rent brændstof?Kredit:Samtalen Energigiganten AGL afslørede i denne uge planer om at producere brintkraft på deres Loy Yang A-kulstation. Men hvordan forvandler vi kul, som ofte opfattes som blot lavet af kulsto -
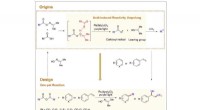 Effektiv metode til fotokatalytiske fluoralkyleringer af (hetero)arenerGrafisk abstrakt. Kredit:Chem Catalysis (2022). DOI:10.1016/j.checat.2022.05.018 Fluoroalkylerede aromatiske forbindelser har egenskaber som permeabilitet, lipofilicitet og metabolisk stabilitet. B
Effektiv metode til fotokatalytiske fluoralkyleringer af (hetero)arenerGrafisk abstrakt. Kredit:Chem Catalysis (2022). DOI:10.1016/j.checat.2022.05.018 Fluoroalkylerede aromatiske forbindelser har egenskaber som permeabilitet, lipofilicitet og metabolisk stabilitet. B
- BHPs aflæsning af olie- og gasaktiver viser, at det globale marked har tændt for fossile brændsto…
- RNA's rolle i tidlig evolution:Hvordan naturlig selektion formede tidlige RNA-molekyler
- Hvordan vil du beskrive cyclotron -bevægelsen?
- DefCon-præsentanter udforsker programmer-de-anonymisering, stilistiske fingeraftryk
- Hvad er den vigtigste kilde til varmeenergi i jordens indre kerne?
- Hvordan finder du ligevægtskonstant ved hjælp af standardreduktionspotentialer?


