Forberedelse af en 2M kaliumchloridopløsning:En trin-for-trin guide
Forstå vilkårene
* Molaritet (M): Repræsenterer koncentrationen af en opløsning. En 2 M opløsning betyder, at der er 2 mol KCl opløst i 1 liter opløsning.
* Fuldvarpe: En måleenhed for mængden af stof.
* KCl: Den kemiske formel for kaliumchlorid.
Materialer
* Fast kaliumchlorid (KCl).
* Destilleret vand
* Gradueret cylinder (250 ml)
* Vægtvægt
* Bægerglas
* Rørestav
Procedure
1. Beregn massen af KCl:
* Molar masse af KCl: 74,55 g/mol (39,10 g/mol for K + 35,45 g/mol for Cl)
* Moler KCl påkrævet: (2 M) * (0,250 L) =0,5 mol
* Nødvendig masse af KCl: (0,5 mol) * (74,55 g/mol) =37,275 g
2. Væg KCl:
* Brug en vægt til nøjagtigt at veje 37,275 gram KCl.
3. Opløs i vand:
* Tilsæt ca. 150 ml destilleret vand til et bægerglas.
* Tilsæt forsigtigt den vejede KCl til vandet og rør, indtil det er helt opløst.
* Når opløsningen er opløst, overføres forsigtigt opløsningen til en 250 ml målecylinder.
* Tilsæt mere destilleret vand til målecylinderen, indtil det samlede volumen når 250 ml.
4. Bland grundigt:
* Rør opløsningen med en rørestav for at sikre, at KCl er helt opløst, og koncentrationen er ensartet.
Vigtige bemærkninger:
* Sikkerhed: Bær altid passende beskyttelsesbriller og handsker ved håndtering af kemikalier.
* Destilleret vand: Brug destilleret eller deioniseret vand for at minimere urenheder, der kan påvirke opløsningens nøjagtighed.
* Opløsning: Opløsningsprocessen kan generere varme. Lad opløsningen køle af til stuetemperatur, før der foretages endelige volumenjusteringer.
Mærkning:
* Mærk opløsningen med følgende oplysninger:
* Kaliumchlorid (KCl)
* Koncentration (2 M)
* Dato udarbejdet
Sig til, hvis du har andre spørgsmål!
Sidste artikelNeutraliserende syrer:Forstå reaktioner og pH-ændringer
Næste artikelKaliumbromid- og fluorreaktion:KF- og Br₂-dannelse
 Varme artikler
Varme artikler
-
 Konvertering af ledningsevne til koncentration:En praktisk vejledningAf Tammie Painter • Opdateret 24. marts 2022 Ledningsevne måler, hvor let en opløsning leder elektrisk strøm, som er direkte knyttet til koncentrationen af tilstedeværende ioner. Ved at anvende en på
Konvertering af ledningsevne til koncentration:En praktisk vejledningAf Tammie Painter • Opdateret 24. marts 2022 Ledningsevne måler, hvor let en opløsning leder elektrisk strøm, som er direkte knyttet til koncentrationen af tilstedeværende ioner. Ved at anvende en på -
 Forskere bruger grønt guld til hurtigt at opdage og identificere skadelige bakterierProfessor Abdennour Abbas og hans forskerhold har udført grundforskning i samspillet mellem guldnanopartikler og celleoverflader for at skabe nye sensorer. Forskelligt formede guldnanopartikler som de
Forskere bruger grønt guld til hurtigt at opdage og identificere skadelige bakterierProfessor Abdennour Abbas og hans forskerhold har udført grundforskning i samspillet mellem guldnanopartikler og celleoverflader for at skabe nye sensorer. Forskelligt formede guldnanopartikler som de -
 Brydning af ammoniak:En ny katalysator til at generere brint fra ammoniak ved lave temperaturer-. Kredit:Tokyo Tech Den nuværende globale klimakrise og vores hurtigt vigende energiressourcer får folk til at kigge efter renere alternativer som brintbrændstof. Ved forbrænding i nærvær af ilt,
Brydning af ammoniak:En ny katalysator til at generere brint fra ammoniak ved lave temperaturer-. Kredit:Tokyo Tech Den nuværende globale klimakrise og vores hurtigt vigende energiressourcer får folk til at kigge efter renere alternativer som brintbrændstof. Ved forbrænding i nærvær af ilt, -
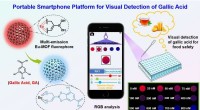 Ny fluorescenssensorplatform udviklet til visuel overvågning af fødevaresikkerhedDen bærbare smartphone-platform baseret på dual-emission Eu-MOF til visuel påvisning af gallussyre i fødevaresikkerheden. Kredit:Pan Lei Et forskerhold ledet af prof. Jiang Changlong fra Institute
Ny fluorescenssensorplatform udviklet til visuel overvågning af fødevaresikkerhedDen bærbare smartphone-platform baseret på dual-emission Eu-MOF til visuel påvisning af gallussyre i fødevaresikkerheden. Kredit:Pan Lei Et forskerhold ledet af prof. Jiang Changlong fra Institute
- Hvordan spreder havbunden støtte kontinental drift?
- Hvorfor varierer titreringskurven med forskellig syrebasetitrering?
- Hvad er nogle funktioner, der giver dig mulighed for at identificere opgravede bjerge?
- Den bemærkelsesværdige fortælling om Wilhelm Röntgens banebrydende røntgenopdagelse
- Jordens skorpeminerogi driver hotspots for intraterrestrisk liv
- Hvad er dyreceller?


