Resonansstrukturer og elektronpunktsformler:Forståelse af gyldige variationer
Antallet af gyldige resonansstrukturer afhænger af selve molekylet eller ionen. Der er ikke noget fast nummer.
Her er grunden:
* Flere bindingsmuligheder: Tilstedeværelsen af delokaliserede elektroner (elektroner, der ikke er begrænset til en enkeltbinding) giver mulighed for forskellige arrangementer af dobbelt- eller tredobbeltbindinger.
* Symmetri: Molekyler med symmetriske strukturer har ofte flere resonansstrukturer.
For eksempel:
* Ozon (O3): Ozon har to resonansstrukturer.
* Nitration (NO3-) :Nitrationen har tre resonansstrukturer.
* Benzen (C6H6): Benzen har to store resonansstrukturer, hvilket bidrager til dets exceptionelle stabilitet.
Vigtig bemærkning:
Resonansstrukturer er ikke forskellige molekyler; de er simpelthen forskellige måder at repræsentere det samme molekyle på. Den faktiske struktur af molekylet er en hybrid af alle resonansstrukturerne, hvor elektronerne delokaliseres over hele molekylet.
 Varme artikler
Varme artikler
-
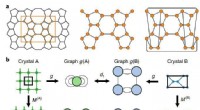 En ny matematisk tilgang til forståelse af zeolitterGraph og supercell matching. en, Repræsentation af en zeolit ved hjælp af en graf (til venstre). Enhedscellegrafen (midten) modificeres for at opfylde periodiske grænsebetingelser ved at sløjfe bind
En ny matematisk tilgang til forståelse af zeolitterGraph og supercell matching. en, Repræsentation af en zeolit ved hjælp af en graf (til venstre). Enhedscellegrafen (midten) modificeres for at opfylde periodiske grænsebetingelser ved at sløjfe bind -
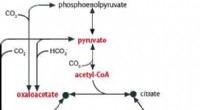 Opdagelse af et oprindeligt metabolisk system, der giver os et glimt af livets oprindelse på JordenFig. 1:Forholdet mellem TCA -cyklussen og pyruvat, acetyl-CoA, oxaloacetat, oxoglutarat, og succinyl-CoA er vist. Kredit:Hokkaido University Multi-omics forskning på Thermosulfidibacter (isoleret
Opdagelse af et oprindeligt metabolisk system, der giver os et glimt af livets oprindelse på JordenFig. 1:Forholdet mellem TCA -cyklussen og pyruvat, acetyl-CoA, oxaloacetat, oxoglutarat, og succinyl-CoA er vist. Kredit:Hokkaido University Multi-omics forskning på Thermosulfidibacter (isoleret -
 Samtale mellem en biolog og en filosof - er mennesket blevet en halvgud?Kredit:karamel/Pixabay To professorer fra universitetet i Lorraine fortsætter de udvekslinger, der tidligere blev indledt i Selvtransformation og religion og Identitet, metamorfose og selvet. Her b
Samtale mellem en biolog og en filosof - er mennesket blevet en halvgud?Kredit:karamel/Pixabay To professorer fra universitetet i Lorraine fortsætter de udvekslinger, der tidligere blev indledt i Selvtransformation og religion og Identitet, metamorfose og selvet. Her b -
 Nobelugen fortsætter med KemiprisenI denne mandag, 10. december, 2018 filbillede, en buste af Nobelprisstifteren, Alfred Nobel udstillet i Koncertsalen under Nobelprisuddelingen i Stockholm. Kontrovers forfølger Nobelpriserne for fred
Nobelugen fortsætter med KemiprisenI denne mandag, 10. december, 2018 filbillede, en buste af Nobelprisstifteren, Alfred Nobel udstillet i Koncertsalen under Nobelprisuddelingen i Stockholm. Kontrovers forfølger Nobelpriserne for fred


