Kuldioxid vs. natriumoxid:En sammenligning af fysiske egenskaber
Culdioxid (CO2)
* Tilstand ved stuetemperatur: Gas
* Udseende: Farveløs og lugtfri
* Tæthed: 1,98 kg/m³ (ved 0 °C og 1 atm)
* Smeltepunkt: -78,5 °C (-109,3 °F) (sublimerer)
* Kogepunkt: -56,6 °C (-69,9 °F)
* Opløselighed i vand: Lidt opløselig (danner kulsyre)
* Konduktivitet: Ikke-ledende (i sin gasform)
Natriumoxid (Na2O)
* Tilstand ved stuetemperatur: Solid
* Udseende: Hvidt, krystallinsk fast stof
* Tæthed: 2,27 g/cm³
* Smeltepunkt: 1275 °C (2327 °F)
* Kogepunkt: 1950 °C (3542 °F)
* Opløselighed i vand: Reagerer voldsomt med vand og danner natriumhydroxid (NaOH)
* Konduktivitet: Ikke-ledende i sin faste form, men kan være ledende, når det opløses i vand (på grund af dannelse af ioner)
Nøgleforskelle:
* Sagens tilstand: CO2 er en gas ved stuetemperatur, mens Na2O er et fast stof.
* Smelte- og kogepunkter: Na2O har meget højere smelte- og kogepunkter end CO2 på grund af de stærke ionbindinger, der holder dets struktur sammen.
* Opløselighed: CO2 er svagt opløseligt i vand, mens Na2O reagerer voldsomt med vand og danner en stærkt alkalisk opløsning.
* Konduktivitet: CO2 er en dårlig leder af elektricitet, mens Na2O kan lede, når det opløses i vand.
Opsummering: Forskellene i fysiske egenskaber mellem kuldioxid og natriumoxid skyldes forskellene i deres bindinger og molekylære strukturer. CO2 er en molekylær forbindelse med svage intermolekylære kræfter, mens Na2O er en ionisk forbindelse med stærke elektrostatiske vekselvirkninger mellem dets ioner.
Sidste artikelKulstof- og kobberoxidreaktion:ordligning og forklaring
Næste artikelForståelse af kemisk toksicitet:Hvilken er den farligste?
 Varme artikler
Varme artikler
-
 Bedre vurdering af bakteriers følsomhed over for antibiotika kan ændre, hvordan lægemidler ordine…En mikrochip-antibiotisk testplatform, der reducerer den nødvendige tid til at identificere den rigtige medicin, udviklet af forskere ved Korea Advanced Institute of Science and Technology. Kredit:Jeo
Bedre vurdering af bakteriers følsomhed over for antibiotika kan ændre, hvordan lægemidler ordine…En mikrochip-antibiotisk testplatform, der reducerer den nødvendige tid til at identificere den rigtige medicin, udviklet af forskere ved Korea Advanced Institute of Science and Technology. Kredit:Jeo -
 En ubrydelig kombination af usynlig blæk og kunstig intelligensMed almindelig blæk, en computer trænet med kodebogen afkoder STOP (øverst); når der vises et UV-lys på papiret, det usynlige blæk er blotlagt, og det rigtige budskab afsløres som BEGIN (nederst). Kre
En ubrydelig kombination af usynlig blæk og kunstig intelligensMed almindelig blæk, en computer trænet med kodebogen afkoder STOP (øverst); når der vises et UV-lys på papiret, det usynlige blæk er blotlagt, og det rigtige budskab afsløres som BEGIN (nederst). Kre -
 At skabe unikke konstruktioner fra metalmembranerCykelbanen Krylatskoye - sportsanlæg i Moskva, i Krylatskoye-distriktet. Kredit:Sergey Krivoshapko RUDN University Professor Sergey Krivoshapko har assimileret information om metalmembran-ophængte
At skabe unikke konstruktioner fra metalmembranerCykelbanen Krylatskoye - sportsanlæg i Moskva, i Krylatskoye-distriktet. Kredit:Sergey Krivoshapko RUDN University Professor Sergey Krivoshapko har assimileret information om metalmembran-ophængte -
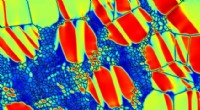 I formhukommelseslegeringer, den rigtige kombination af krystalkorn kan opnå høj styrke og stadig …Simuleret formhukommelsesfaseovergang i en formhukommelseslegering med små og store krystalkorn. Kredit:IOP Publishing A*STAR forskere har vist, gennem en supercomputersimulering, at høj styrke og
I formhukommelseslegeringer, den rigtige kombination af krystalkorn kan opnå høj styrke og stadig …Simuleret formhukommelsesfaseovergang i en formhukommelseslegering med små og store krystalkorn. Kredit:IOP Publishing A*STAR forskere har vist, gennem en supercomputersimulering, at høj styrke og
- Ikke hjemme? Walmart vil gerne gå ind og opbevare dit køleskab
- Former deuterium i D2O brintbindinger?
- Hvad finder sted i cellerne, når det bevæger sig fra saltvand til ferskvand?
- Usædvanlige fakta om skov økosystemet
- EU -lovgivere presser på for cybersikkerhed, datarevision af Facebook
- Hvilke tre ting klassificerer geolog klipper baseret på?


