Beregning af normalitet:Bestemmelse af Na₂CO₃-masse for en 0,02 N opløsning
Forstå normalitet (N)
* Normalitet er en koncentrationsenhed, der måler antallet af ækvivalenter af et opløst stof pr. liter opløsning.
* En ækvivalent er mængden af et stof, der kan reagere med eller erstatte ét mol hydrogenioner (H⁺) eller hydroxidioner (OH⁻).
Na₂CO₃ og ækvivalenter
* Natriumcarbonat (Na₂CO₃) er en base. Når det opløses i vand, reagerer det med vand og producerer carbonationer (CO₃²⁻), som kan acceptere to hydrogenioner (H⁺).
* Derfor svarer et mol Na2CO3 til to ækvivalenter (fordi det kan acceptere to mol H⁺).
Beregning af den nødvendige masse
1. Molar masse af Na2C03: 105,99 g/mol
2. Ækvivalenter pr. mol: 2 ækvivalenter/mol (som forklaret ovenfor)
3. Ønsket normalitet: 0,02 N
4. Opløsningsvolumen: 1 L
Beregninger:
* Gram Na₂CO₃ påkrævet: (0,02 N) * (1 L) * (105,99 g/mol) / (2 ækvivalenter/mol) =1,06 g
Konklusion
Tilsætning af 1,06 g Na2CO3 til 1 liter vand giver en 0,02 N opløsning, fordi denne masse giver det korrekte antal ækvivalenter af Na2CO3 for at opnå den ønskede normalitet.
Sidste artikelJerncarbonat og myresyrereaktion:Kemisk ligning og forklaring
Næste artikelEr kuldioxid et oxid? Forstå dens sure egenskaber
 Varme artikler
Varme artikler
-
 Microgel-pulver bekæmper infektioner og hjælper med at hele sårMicrogel Powder:Sticky catechol laver hydrogenperoxid; Sikker og tør:Opbevaring af flydende brintoverilte kan være farligt, inert pulver er mere bærbart; Neutral pH:Tilsætning af en let bufret opløsni
Microgel-pulver bekæmper infektioner og hjælper med at hele sårMicrogel Powder:Sticky catechol laver hydrogenperoxid; Sikker og tør:Opbevaring af flydende brintoverilte kan være farligt, inert pulver er mere bærbart; Neutral pH:Tilsætning af en let bufret opløsni -
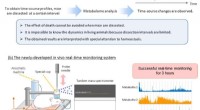 Realtidsdækning af hjernens indre muliggjortFig. 1 Forskelle mellem konventionel metabolomanalyse for dissekerede hjerneprøver og det nyudviklede in vivo realtidsovervågningssystem. Kredit:Nagoya University Overvågning i realtid af dynamikk
Realtidsdækning af hjernens indre muliggjortFig. 1 Forskelle mellem konventionel metabolomanalyse for dissekerede hjerneprøver og det nyudviklede in vivo realtidsovervågningssystem. Kredit:Nagoya University Overvågning i realtid af dynamikk -
 Syntetisere en ny klasse af bio-inspirerede, lysfangende nanomaterialerPOSS-peptoidmolekyler samler sig selv til rombeformede nanokrystaller. Kredit:Stephanie King | Pacific Northwest National Laboratory Inspireret af naturen, forskere ved Pacific Northwest National
Syntetisere en ny klasse af bio-inspirerede, lysfangende nanomaterialerPOSS-peptoidmolekyler samler sig selv til rombeformede nanokrystaller. Kredit:Stephanie King | Pacific Northwest National Laboratory Inspireret af naturen, forskere ved Pacific Northwest National -
 Undersøge vand af en elektrificerende årsagKAUST-forskere observerede, at vedhængende dråber dannet fra hydrofobe kapillærer til ensartede elektriske felter. Kredit:KAUST; Anastasia Serin Et eksperiment, elegant i sin enkelhed, hjælper med
Undersøge vand af en elektrificerende årsagKAUST-forskere observerede, at vedhængende dråber dannet fra hydrofobe kapillærer til ensartede elektriske felter. Kredit:KAUST; Anastasia Serin Et eksperiment, elegant i sin enkelhed, hjælper med


