Balancering af ioniske ligninger:Al + HCl - En trin-for-trin guide
1. Skriv den ubalancerede molekylære ligning:
2 Al(s) + 6 HCl(aq) → 2 AlCl3(aq) + 3 H2(g)
2. Identificer tilskuer-ionerne:
Tilskuerioner er ioner, der optræder på begge sider af ligningen og ikke deltager i den faktiske reaktion. I dette tilfælde er chloridionerne (Cl⁻) tilskuerioner.
3. Skriv hele den ioniske ligning:
2 Al(s) + 6 H+(aq) + 6 Cl⁻(aq) → 2 Al3+(aq) + 6 Cl⁻(aq) + 3 H2(g)
4. Annuller tilskuerionerne:
2 Al(s) + 6 H+(aq) → 2 Al3+(aq) + 3 H2(g)
5. Forenkle ligningen:
Al(s) + 3 H⁺(aq) → Al3⁺(aq) + 3/2 H2(g)
Dette er den afbalancerede ioniske ligning for reaktionen mellem aluminium og saltsyre.
Nøglepunkter:
* Aluminium (Al) er et solidt metal.
* Saltsyre (HCl) er en vandig opløsning.
* Aluminiumchlorid (AlCl3) er en vandig opløsning.
* Brintgas (H₂) produceres som en gas.
* Koefficienterne i den balancerede ligning sikrer, at antallet af atomer i hvert grundstof er det samme på begge sider af ligningen.
 Varme artikler
Varme artikler
-
 Hormonernes universelle sprogElena Bencurova analyserede 123 organismer og udsatte deres proteiner for detaljerede motivanalyser. Kredit:Julius-Maximilians-Universität Würzburg, JMU Bioinformatikspecialister fra universitetet
Hormonernes universelle sprogElena Bencurova analyserede 123 organismer og udsatte deres proteiner for detaljerede motivanalyser. Kredit:Julius-Maximilians-Universität Würzburg, JMU Bioinformatikspecialister fra universitetet -
 Video:Hvordan superhydrofobe materialer forbliver helt tørreKredit:The American Chemical Society Regnfrakker, bil forruder, Vandtætte telefoner:De bruger alle lidt kemi for at forblive tørre. Inspireret af naturen, kemikere bruger ekstremt vand-frygt, elle
Video:Hvordan superhydrofobe materialer forbliver helt tørreKredit:The American Chemical Society Regnfrakker, bil forruder, Vandtætte telefoner:De bruger alle lidt kemi for at forblive tørre. Inspireret af naturen, kemikere bruger ekstremt vand-frygt, elle -
 Farveskiftende sensor registrerer tegn på øjenskade i tårerForskere udviklede en hurtigfølende gel til at måle en molekylær markør for øjenskade i en dråbe. Fra venstre:Carle øjenlæge Dr. Leanne Labriola, Illinois-gæsteforsker Ketan Dighe og professor Dipanja
Farveskiftende sensor registrerer tegn på øjenskade i tårerForskere udviklede en hurtigfølende gel til at måle en molekylær markør for øjenskade i en dråbe. Fra venstre:Carle øjenlæge Dr. Leanne Labriola, Illinois-gæsteforsker Ketan Dighe og professor Dipanja -
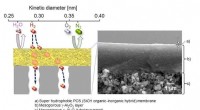 Ny brintbrændstofrensningsmembran baner vejen for en grønnere fremtidEt tværsnitsbillede af selektiv hydrogengennemtrængning i en superhydrofob membran dannet på en porøs rørformet understøtning. Kredit:Yuji Iwamoto fra Nagoya Institute of Technology Brint er bleve
Ny brintbrændstofrensningsmembran baner vejen for en grønnere fremtidEt tværsnitsbillede af selektiv hydrogengennemtrængning i en superhydrofob membran dannet på en porøs rørformet understøtning. Kredit:Yuji Iwamoto fra Nagoya Institute of Technology Brint er bleve
- Hvad drives af atomkraft?
- Hvad er dimensionerne af rotationshastigheden?
- Celledelingsstadium, hvor kromosomer stiller op midt i cellen?
- Bruger mennesker iltgas og udånder kuldioxidgas?
- NASA -rumfartøjer slår rekord for at komme tættest på Solen
- Nanoenheder viser, hvordan celler ændrer sig med tiden, ved at spore indefra


