Sammensætningsstøkiometri:formler, procenter og empiriske/molekylære forhold
Kompositionsstøkiometri:Forståelse af materiens byggesten
Sammensætningsstøkiometri er den gren af kemi, der fokuserer på kvantitative sammenhænge mellem elementer i en sammensætning . Det handler om at bestemme:
* Elemental sammensætning: Masseprocenten af hvert grundstof til stede i en forbindelse.
* Empirisk formel: Det enkleste hele talforhold mellem atomer i en forbindelse.
* Molekylformel: Det faktiske antal atomer af hvert grundstof i et molekyle af forbindelsen.
Nøglebegreber:
* Molar masse: Massen af et mol af et stof (udtrykt i gram/mol).
* Procentsammensætning: Massen af hvert grundstof i en forbindelse udtrykt som en procentdel af den samlede masse.
* Empirisk formelbestemmelse:
* Beregn mol af hvert tilstedeværende element.
* Divider hver molværdi med den mindste molværdi.
* Hvis de resulterende forhold ikke er hele tal, skal du gange dem med en faktor for at få hele tal.
* Molekylformelbestemmelse:
* Bestem den empiriske formel.
* Find molmassen af den empiriske formel.
* Divider den kendte molære masse af forbindelsen med den empiriske formel molær masse.
* Multiplicer sænkningen af den empiriske formel med den resulterende faktor.
Applikationer:
* Analyse af ukendte forbindelser: Bestemmelse af grundstofsammensætningen af en prøve for at identificere dens bestanddele og deres relative mængder.
* Beregning af kemiske reaktioner: Forståelse af støkiometrien af reaktioner for at forudsige mængden af involverede reaktanter og produkter.
* Design af nye materialer: Valg af specifikke elementer og deres forhold for at opnå ønskede egenskaber i materialer.
Eksempel:
Lad os overveje vand (H₂O).
* Elemental sammensætning: 11,19% hydrogen og 88,81% oxygen efter masse.
* Empirisk formel: H2O (som også er molekylformlen i dette tilfælde)
* Molekylformel: H2O
I det væsentlige giver sammensætningsstøkiometri rammerne for at forstå den nøjagtige sammensætning af forbindelser og bruge denne information til at analysere og forudsige kemisk adfærd.
 Varme artikler
Varme artikler
-
 Fanget på fersk gerning:Nøgle kemiske mellemprodukter i forurenende-til-brændstof-reaktion identi…Forskere fra University of Tsukuba og samarbejdspartnere målte eksperimentelt hydrogenering af metaladsorberet formiat. Denne udvikling vil lette praktisk omdannelse af kuldioxidforurenende stof til m
Fanget på fersk gerning:Nøgle kemiske mellemprodukter i forurenende-til-brændstof-reaktion identi…Forskere fra University of Tsukuba og samarbejdspartnere målte eksperimentelt hydrogenering af metaladsorberet formiat. Denne udvikling vil lette praktisk omdannelse af kuldioxidforurenende stof til m -
 Et nyt materiale til fremtidens batteriUCLouvains forskere opdagede et nyt højtydende og sikkert batterimateriale (LTPS), der kan fremskynde opladning og afladning til et niveau, der aldrig er observeret hidtil. Kredit:University of Louvai
Et nyt materiale til fremtidens batteriUCLouvains forskere opdagede et nyt højtydende og sikkert batterimateriale (LTPS), der kan fremskynde opladning og afladning til et niveau, der aldrig er observeret hidtil. Kredit:University of Louvai -
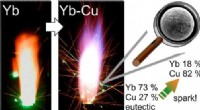 Forskere bruger sjældne jordarters metaller i legeringspulvere til at producere grønne, iøjnefald…Grafisk abstrakt. Kredit:ACS Omega (2022). DOI:10.1021/acsomega.2c03081 Stjernekastere kan være meget sjove - glimtende, brusende og spyttede lysbuer ud fra håndholdte pinde eller rør på jorden. Me
Forskere bruger sjældne jordarters metaller i legeringspulvere til at producere grønne, iøjnefald…Grafisk abstrakt. Kredit:ACS Omega (2022). DOI:10.1021/acsomega.2c03081 Stjernekastere kan være meget sjove - glimtende, brusende og spyttede lysbuer ud fra håndholdte pinde eller rør på jorden. Me -
 Høst rent brintbrændstof gennem kunstig fotosynteseDet farvede elektronmikroskopbillede viser galliumnitridtårnene i den kunstige fotosynteseanordning ved 52,5k forstørrelse. Disse nanostrukturer river vandmolekyler fra hinanden til brint og ilt for a
Høst rent brintbrændstof gennem kunstig fotosynteseDet farvede elektronmikroskopbillede viser galliumnitridtårnene i den kunstige fotosynteseanordning ved 52,5k forstørrelse. Disse nanostrukturer river vandmolekyler fra hinanden til brint og ilt for a
- Hvad er Angel Alcalas videnskabelige holdning?
- Ny undersøgelse præsenterer hygroskopiske mikro/nanolenses langs kulstof nanorør-ionkanaler
- Er kategorierne dyr som plante eller svamp nyttige til klassificering af protister?
- Tung, kortvarig elementarpartikel kunne hjælpe med at forfine forståelsen af universet
- I øjet på en stjernecyklon:En tikkende bombestjernes bizarre hemmeligheder
- Hvordan kan du se, om en kemisk ligning repræsenterer kondensationssyntese?


