Natriumbicarbonat og saltsyrereaktion:kemi forklaret
Reaktionen:
NaHCO₃ (vandigt) + HCl (vandigt) → NaCl (vandigt) + H₂O (l) + CO₂ (g)
Forklaring:
* Syre-base neutralisering: Saltsyren (HCl) er en stærk syre, og natriumhydrogencarbonat (NaHCO₃) er en svag base. Reaktionen er i det væsentlige en neutraliseringsreaktion, hvor syren og basen reagerer for at danne salt og vand.
* Danning af natriumchlorid: Natriumionen (Na⁺) fra NaHC03 kombineres med chloridionen (Cl⁻) fra HCl for at danne natriumchlorid (NaCl), et almindeligt salt.
* Danning af vand: Hydrogenionen (H+) fra HCl kombineres med hydrogencarbonationen (HCO3⁻) fra NaHC03 for at danne kulsyre (H2CO3). Kulsyre er ustabil og nedbrydes hurtigt til vand (H₂O) og kuldioxid (CO₂).
* Udvikling af kuldioxid: Kuldioxid-gassen (CO₂) frigives, hvorfor du observerer brusende eller boblende, når denne reaktion opstår.
Observationer:
* Brusende: Frigivelsen af kuldioxidgas forårsager synlig brusen eller bobler i reaktionsblandingen.
* Varmeproduktion: Reaktionen er eksoterm, hvilket betyder, at den frigiver varme, og opløsningen vil føles varm.
* Ændring i pH: Opløsningens pH vil falde, når saltsyren neutraliseres.
Anvendelser:
Denne reaktion har flere anvendelser:
* Antacida: Natriumbicarbonat bruges i antacida, fordi det neutraliserer mavesyre (HCl).
* Bagning: Reaktionen er ansvarlig for stigningen i brød og andet bagværk.
* Kemisk syntese: Reaktionen bruges i kemisk syntese til at producere natriumchlorid og andre forbindelser.
Sikkerhed:
Saltsyre er et ætsende stof, så det er vigtigt at håndtere det med omtanke. Bær altid passende sikkerhedsudstyr og arbejd i et godt ventileret område.
 Varme artikler
Varme artikler
-
 Ny katalysator til brintproduktion er et skridt mod rent brændstofForsiden viser produktionen af brintgas, når elektroner og protoner mødes på ruthenium-ion-komplekserede grafitiske carbonnitrid-nanoark understøttet på grafenoverfladen. Billedet er baseret på en g
Ny katalysator til brintproduktion er et skridt mod rent brændstofForsiden viser produktionen af brintgas, når elektroner og protoner mødes på ruthenium-ion-komplekserede grafitiske carbonnitrid-nanoark understøttet på grafenoverfladen. Billedet er baseret på en g -
 Et nyt design til flow-batterierOpsætningen til at teste cellen af vanadium redox flow batteri. MEA er monteret på et stativ over den peristaltiske pumpe. Tankene er fyldt med vanadiumelektrolyt (før start af opladning). Kredit:St
Et nyt design til flow-batterierOpsætningen til at teste cellen af vanadium redox flow batteri. MEA er monteret på et stativ over den peristaltiske pumpe. Tankene er fyldt med vanadiumelektrolyt (før start af opladning). Kredit:St -
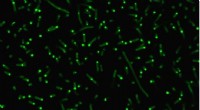 Forskere skaber kunstige organeller for at kontrollere cellulær adfærdIntrinsisk forstyrrede proteiner (fluorescerende grønt) klumper sig sammen i celler for at danne kunstige organeller. Kredit:Duke University Biomedicinske ingeniører ved Duke University har demons
Forskere skaber kunstige organeller for at kontrollere cellulær adfærdIntrinsisk forstyrrede proteiner (fluorescerende grønt) klumper sig sammen i celler for at danne kunstige organeller. Kredit:Duke University Biomedicinske ingeniører ved Duke University har demons -
 En mulig afslutning på evige kemikalierKredit:Marla Bereni/UCR Syntetiske kemikalier kendt som per- og polyfluoralkyler, eller PFAS, indeholder bindinger mellem kulstof- og fluoratomer, der anses for at være de stærkeste i organisk kem
En mulig afslutning på evige kemikalierKredit:Marla Bereni/UCR Syntetiske kemikalier kendt som per- og polyfluoralkyler, eller PFAS, indeholder bindinger mellem kulstof- og fluoratomer, der anses for at være de stærkeste i organisk kem
- Alt, hvad der har masse og tager plads?
- Forskning i perovskit-silicium tandemceller viser ny vej at gå
- I nuklear fusion, hvilke atomer bruges til at producere helium med større masser?
- Hvad skaber ladningen i en elektrisk strøm?
- 100 mest truede arter:Er de uvurderlige eller værdiløse?
- Hvad gør et bjergbjerge?


