Forståelse af ioniske bindinger:Dannelse, egenskaber og eksempler
* Metaller har tendens til at miste elektroner og bliver til positivt ladede ioner (kationer).
* Ikke-metaller har tendens til at få elektroner og bliver negativt ladede ioner (anioner).
Traktionen mellem disse modsat ladede ioner er det, der danner ionbindingen.
Nøglepunkter:
* Elektronegativitetsforskel: Ionbindinger dannes, når elektronegativitetsforskellen mellem de to atomer er stor. Elektronegativitet er et mål for et atoms evne til at tiltrække elektroner.
* Overførsel af elektroner: Metalatomet donerer en eller flere elektroner til ikke-metalatomet, hvilket skaber en komplet ydre skal for begge.
* Elektrostatisk attraktion: De resulterende ioner holdes sammen af stærke elektrostatiske kræfter.
Eksempler:
* Natriumchlorid (NaCl): Natrium (Na), et metal, mister en elektron til klor (Cl), et ikke-metal. Den resulterende positivt ladede natriumion (Na+) og negativt ladede chloridion (Cl-) tiltrækker hinanden og danner en ionbinding.
* Magnesiumoxid (MgO): Magnesium (Mg), et metal, mister to elektroner til oxygen (O), et ikke-metal. Den resulterende positivt ladede magnesiumion (Mg2+) og negativt ladede oxidion (O2-) tiltrækker hinanden og danner en ionbinding.
Karakteristika for ioniske forbindelser:
* Høje smelte- og kogepunkter: På grund af de stærke elektrostatiske kræfter, der holder dem sammen.
* Krystallinsk struktur: Ioniske forbindelser danner et regelmæssigt, gentaget mønster i deres faste tilstand.
* Konduktivitet: Ioniske forbindelser leder elektricitet, når de smeltes eller opløses i vand, da ionerne bliver mobile.
* Skørt: Ioniske forbindelser er skøre, fordi ionerne er arrangeret i en stiv struktur. En stærk kraft kan forstyrre denne struktur, hvilket får forbindelsen til at bryde.
Sidste artikelKemikalier, der ødelægger stof:En guide til almindelige skader
Næste artikelNatriumhydroxid:Forståelse af lud og kaustisk soda
 Varme artikler
Varme artikler
-
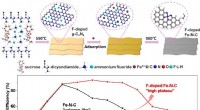 Forskere bruger fluor-dopingmetode til at konstruere katalysatorer med forbedret ydeevneDen F-dopede Fe-N-C enkeltstedskatalysator bevarer fordelen ved lavt overpotentiale for Fe-N-C med meget øget CO faradaisk effektivitet og delvis strømtæthed på grund af den stabiliserede Fe3+ aktive
Forskere bruger fluor-dopingmetode til at konstruere katalysatorer med forbedret ydeevneDen F-dopede Fe-N-C enkeltstedskatalysator bevarer fordelen ved lavt overpotentiale for Fe-N-C med meget øget CO faradaisk effektivitet og delvis strømtæthed på grund af den stabiliserede Fe3+ aktive -
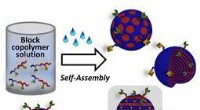 Oprettelse og selektiv funktionalisering af viruslignende polymerpartiklerSkematisk illustration af værket. Kredit:John Wiley &Sons, Inc. Forskere ved Tohoku University i Japan har samarbejdet med andre for at udvikle en enkel måde at skabe og funktionalisere virusligne
Oprettelse og selektiv funktionalisering af viruslignende polymerpartiklerSkematisk illustration af værket. Kredit:John Wiley &Sons, Inc. Forskere ved Tohoku University i Japan har samarbejdet med andre for at udvikle en enkel måde at skabe og funktionalisere virusligne -
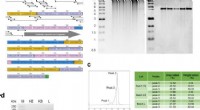 Rekombinant kollagenpolypeptid som et alsidigt knogletransplantatbiomaterialeMolekylært design og syntese af rekombinant polypeptid RCPhC1. (a) Peptidsekvensen af RCPhC1 viser Gly-Xaa-Yaa-gentagelser med aminosyresubstitutioner (rød). Alle peptidfragmenter (minimum penta-sek
Rekombinant kollagenpolypeptid som et alsidigt knogletransplantatbiomaterialeMolekylært design og syntese af rekombinant polypeptid RCPhC1. (a) Peptidsekvensen af RCPhC1 viser Gly-Xaa-Yaa-gentagelser med aminosyresubstitutioner (rød). Alle peptidfragmenter (minimum penta-sek -
 Flere elektroniske materialer åbnede op med nye metal-organiske rammerProfessor Richard Walton, University of Warwick. Kredit:University of Warwick Flere materialer til elektroniske applikationer kunne identificeres, takket være opdagelsen af en ny metal-organisk
Flere elektroniske materialer åbnede op med nye metal-organiske rammerProfessor Richard Walton, University of Warwick. Kredit:University of Warwick Flere materialer til elektroniske applikationer kunne identificeres, takket være opdagelsen af en ny metal-organisk
- teori om personlighed kaldes en trepartsmodel Hvad betyder det?
- Fakta om stokken Caterpillar
- Når celler ikke har brug for energi, når ATP er rigelig acetyl COA kan konverteres til?
- Forståelse af produkterne af lysuafhængige reaktioner (Calvin-cyklus)
- Hvad er vægten af et 25 kg objektligningsmatematik svar med ordentlige enheder?
- Forfader til middelhavsmosaikker opdaget i Tyrkiet


