Rekombinant kollagenpolypeptid som et alsidigt knogletransplantatbiomateriale
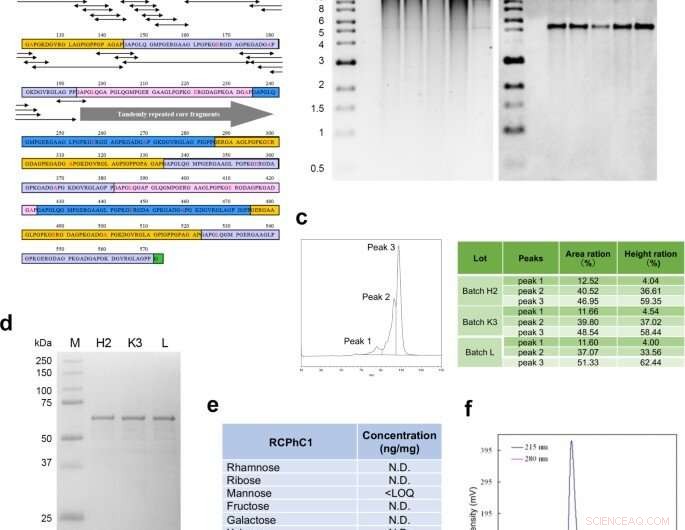
Molekylært design og syntese af rekombinant polypeptid RCPhC1. (a) Peptidsekvensen af RCPhC1 viser Gly-Xaa-Yaa-gentagelser med aminosyresubstitutioner (rød). Alle peptidfragmenter (minimum penta-sekvenser) indeholdende aminosyresubstitutionerne (dobbelte hovedpile) blev matchet med humane kollagensekvenser. (b) Genomisk DNA-stabilitet i arbejdscellebanken. Efter hver af fire på hinanden følgende fragmenteringer, genomisk DNA blev isoleret (bane 1-4) og sammenlignet med det originale genomiske DNA (bane 5). Det højre panel, Southern blot hybridiseret med AOX1-promotorproben. (c) Reproducerbarheden blev analyseret ved væskekromatografi. Omvendt fase-profilen viste tre toppe, som konsekvent blev identificeret i tre forskellige batches (H2, K3, og L). (d) Reproducerbarhed blev også evalueret af SDA-PAGE. Det enkelte bånd af tre forskellige partier antydede også fraværet af post-translationel modifikation. (e) Fraværet af post-translationel glycosylering. (f) Gelpermeationskromatografi bekræftede den høje renhed af RCPhCl. Kredit:Nature Communications Materials, doi:10.1038/s43246-020-00089-9
Den nuværende guldstandard for knogletransplantationskirurgi inkluderer autografts og allografts, selvom der er en stigende efterspørgsel efter at udvikle syntetiske biomaterialer til forbedret bio-integration i knoglevævsteknologi. I en ny rapport, der nu er offentliggjort den Naturkommunikationsmaterialer , Hideo Fushimi og et forskerhold inden for biovidenskab og teknik, og rekonstruktiv bioteknologi i Japan og USA, udviklet et bionedbrydeligt stilladsmateriale ved hjælp af rekombinante proteiner eller polypeptider som en kilde til hydrogel-baserede graftmaterialer. Holdet brugte human type I kollagen alfa 1-kæde (forkortet RCPhC1) som en kilde til at udvikle det rekombinante polypeptid og demonstrerede fleksibiliteten af materialet til at konstruere ideelle egenskaber for knogletransplantater. Holdet udviklede også RCPhC1 knogletransplantater ved hjælp af en meget skalerbar, strømlinet produktionsprotokol til den robuste generering af modent knoglevæv i laboratoriet. Knogletransplantatet resorberes fuldstændigt efter vævsregenerering i en præklinisk dyremodel for effektiv biologisk integration.
Knoglevævsteknik med biomimetik, syntetiske knogletransplantater
I dette arbejde, Fushimi et al. udviklet et syntetisk knogletransplantatmateriale ved at bruge et rekombinant protein forkortet RCPhC1. Udviklingen giver et alsidigt kildemateriale til fremstilling af syntetiske knogletransplantater via fleksibel teknik. Ved at bruge prækliniske undersøgelser i knogledefektmodeller hos hunde og gnavere, holdet viste forbedret effektivitet af knogletransplantaterne til at regenerere knoglevæv med strukturel modenhed. I klinisk ortopædi, tab af vævsvolumen og funktion er et kendetegn for skade, kronisk betændelse, og metabolisk og genetisk sygdom. Mens knoglevæv aktivt kan regenerere via proliferation og osteogen differentiering af mesenkymale stromale eller stamceller, store knogledefekter kræver kirurgiske indgreb for at reparere og genopbygge knogler med knogletransplantatmaterialer.
Globalt, ortopædkirurger udfører cirka 2,2 millioner knogletransplantationsprocedurer årligt på et ekstremt dyrt globalt marked. Menneskets knoglevæv er sammensat af organisk ekstracellulær matrix, krystalliserede calcium- og fosformineraler, der danner hydroxyapatit. Knogletransplantatmaterialer kan efterligne strukturen og den biokemiske sammensætning af knoglevæv. Ortopædkirurger og forskere har brugt autologe knogletransplantater (celler og væv opnået fra det samme individ) til at reparere knogledefekter på grund af mineralske og immunologiske bekymringer, selvom komplikationer på operationsstederne kan føre til alternative transplantationsmetoder såsom allotransplantater (celler og væv opnået fra et andet individ). Den nyere udvikling af biomimetik, syntetiske biomaterialer til knoglevævsteknologi imødekommer et presserende behov i sundhedssektoren for at udvikle nye graftmaterialer uden brug af menneske- eller dyrevæv.
Tekniske kontrolfaktorer til udvikling af isotropiske is-templatede strukturer ved tyndtlags frysestøbning (TLFC). (a) Diagram over frysestøbeapparat. (b) Typisk temperaturmåling af bunden af kølekoppen (blå) og overfladen af opløst stof (rød) under frysestøbningsprocessen. Der var en signifikant uoverensstemmelse mellem kølebægeret og overfladen af det opløste stof under fryseperioden. (c) Diagram af anisotropisk is-template struktur og den faktiske RCPhC1 mikrostruktur, der indeholder den lille pore zone. Skala bar er lig med 500 μm. d TLFC reducerede temperaturforskellen mellem kølekoppen (blå) og overfladen af opløst stof (rød) under fryseperioden. (e) Effekten af minimumstemperatur og afkølingsvarighed på den isotrope indre porestruktur. Den ensartede porestruktur (blå) udviklede sig, når minimumstemperaturen var under -10 °C, men blev ikke påvirket af varigheden af afkøling. Den uregelmæssige indre porestruktur (rød) udviklede sig oftere, når minimumstemperaturen var over -10 °C. Skala bar er lig med 500 μm. Grønt område viser antallet af ensartede frysetørrede kager. Rødt område viser antallet af uregelmæssigt frysetørrede kager. (f) Virkningen af bloktemperaturen på den indre porestørrelse. Diamanter viser medianværdier. De lavere bloktemperaturer øgede antallet af små porer. Skala bar er lig med 500 μm. (g) Den indre struktur udviklet af omrøringen (røde cirkler), anisotropiske (grønne cirkler) og isotrope (blå cirkler) frysestøbningsmetoder blev evalueret ved vandabsorptions- og syrenedbrydningsanalyser. RCPhC1-svampe blev foreløbigt dehydrotermisk tværbundet ved 130 °C i 7 timer. Blå linjer i felt b og d angiver temperaturregistreringen fra termoelementet i bunden af opløsningerne. Røde linjer indikerer det ved overfladen af opløsningen. Kredit:Nature Communications Materials, doi:10.1038/s43246-020-00089-9 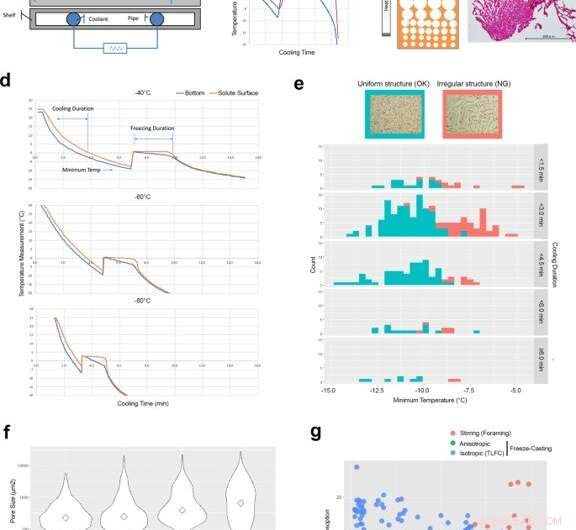
Holdet brugte type I kollagen, rigeligt udtrykt i bindevæv og interstitielle membraner som en væsentlig organisk komponent i knoglevæv. Proteinsekvensen af type I kollagen spiller en vigtig rolle i etableringen af den mekaniske styrke af knogler. Holdet klonede først det komplementære DNA (cDNA) - en DNA-kopi af et messenger RNA (mRNA) molekyle, der koder for polypeptidet (proteinsekvensen) RCPhC1, ind i en ekspressionsvektor. For at opnå dette, de brugte en methylotrofisk gærart kendt som Pichia pastoris til at overføre sekvensen og generere master- og arbejdscellebanker. Holdet bekræftede aminosyresammensætningen af det syntetiske polypeptid og karakteriserede produktet grundigt.
De konstruerede derefter den indre struktur af transplantatmaterialet til at opfylde specifikke krav til målvævet. For at skabe en ensartet porestruktur, derfor, Fushimi et al. designet en tynd-lags frysestøbning (TLFC) protokol. Den alsidige frysetilgang genererede et stort antal porer med tynde vægge for at danne et isotropt RCPhC1-stillads med forskellige interne strukturer.
Tekniske faktorer, der påvirker dehydrotermisk tværbinding af RCPhC1 for at kontrollere biologisk nedbrydningshastighed og mekanisk styrke. (a) Virkningen af tværbindingstemperatur og tværbindingsvarighed på bionedbrydningshastigheden vurderet ved in vitro syrenedbrydningsanalyse. (b) Tværbindingstemperatur påvirkede ikke lineært syrenedbrydningsoverlevelseshastigheden. I betragtning af den efterfølgende sterilisering, tværbindingstemperaturen blev sat til 130°C. (c) Tværbindingsvarighed blev fundet at være den dominerende kontrolfaktor, hvilket lineært øgede syrenedbrydningsoverlevelsesraten for RCPhC1 op til 10 t. Svinegelatinemateriale reagerede på samme måde på tværbindingsvarigheden, selvom det kræver meget længere varighed. (d) Fysisk egenskab ved dehydrotermisk tværbundet RCPhC1. Den tilsvarende fysiske egenskab af dehydrotermisk tværbundet porcin gelatine krævede 10 gange længere tværbindingsvarighed. (e) Den mekaniske styrke af dehydrotermisk tværbundet RCPhC1 (130 °C, 7 h) var signifikant højere end for dehydrotermisk tværbundet svinegelatine (130 °C, 72 t). Fejlbjælke repræsenterer s.d. (f) Dehydrotermisk tværbundet RCPhC1 (130 °C, 7 h) blev behandlet med trypsin og udsat for højtydende LC. Co-migrering af peptidfragmenter indikerede flere tværbindingssteder. Kredit:Nature Communications Materials, doi:10.1038/s43246-020-00089-9 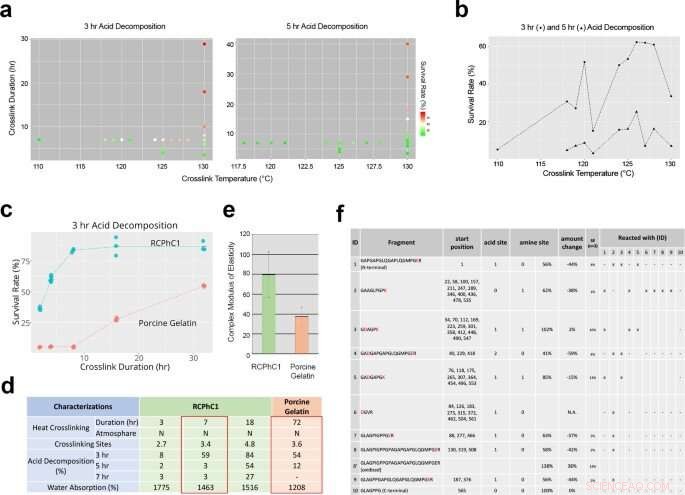
Fushimi et al. derefter udsat materialet for dehydrotermisk tværbindingsbehandling for at teste virkningen af tværbindingstemperatur og varighed på dets sammensætning. Efter at have testet nedstrømsproduktet for mikrobiel kontaminering, temperaturen under fremstillingsprocessen blev bekræftet at være effektiv til tørvarmesterilisering. Yderligere test viste, hvordan den unikke aminosyresammensætning af det rekombinante protein bidrog til dets robuste hydrotermiske tværbindingseffektivitet. Holdet optimerede derefter det rekombinante proteinmateriale til knogletransplantation ved at regulere koncentrationen af polypeptidmaterialet og dets frysetemperatur baseret på volumenet af transplantat-induceret knogle i en rotte calvarial (kranie) knogledefekt model. Fire uger efter podning af materialet i dyremodellen, holdet brugte mikrocomputertomografi (micro CT)-baseret knoglevolumen estimering. Resultaterne indikerede en optimal koncentration på 7,5 procent RCPhC1, en frysetemperatur på -40 til -60 grader Celsius, og dehydrotermisk tværbinding ved 130 °C i 7 timer for at være bedst egnet til fremstilling af rekombinant knogletransplantatmateriale.
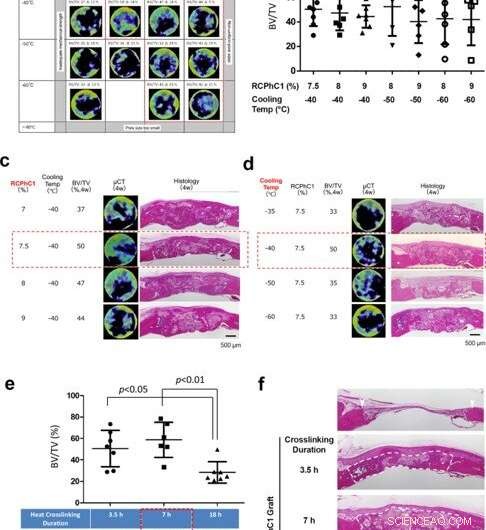
Optimering af tekniske kontrolfaktorer. (a) Optimering af kombinerede faktorer for RCPhC1-koncentration af opløst stof og TLFC-bloktemperatur, med den foreløbige dehydrotermiske tværbinding ved 130°C i 7 timer. Det optimale område blev indsnævret til RCPhC1-koncentration mellem 7,5 og 9% og TLFC-bloktemperatur mellem -40 og -60 °C (rød prikket blok). (b) BV/TV-målinger inden for gruppen af det optimale område for RCP1C1-koncentration og køletemperatur. Der var ingen statistisk forskel mellem grupperne. (c) Virkningen af RCPhCl-koncentration af opløst stof på knogleregenerering. Skala bar er lig med 500 μm. (d) Effekten af TLFC-bloktemperatur på knogleregenerering. Skala bar er lig med 500 μm. (e) Virkningen af dehydrotermisk tværbindingsvarighed på knogledannelse. (n = 7; Tukeys multiple sammenligningstest) (f). Effekten af dehydrotermisk tværbindingsvarighed på vedligeholdelsen af sårhelingsrum i rotte calvarial knogledefekt. Hvide pilespidser viser defekte kanter. Hvide stiplede linjer kredser om nydannet væv. Skala bar er lig med 500 μm. Vandrette linjer i b, og e repræsenterer middel ± s.d. Kredit:Nature Communications Materials, doi:10.1038/s43246-020-00089-9
Robust regenerering af vitalt knoglevæv i prækliniske modeller med graftmaterialer
Baseret på de eksperimentelt verificerede optimale forhold, Fushimi et al. fremstillet RCPhC1-knogletransplantaterne med porøse granulat. Ved at bruge modellen af rotte-calvarial knogledefekt, de viste, hvordan knogletransplantatet robust inducerede knogleregenerering i den indre porestruktur, mens den gradvist nedbrydes in vivo, at angive biokompatibilitet og effektiv biointegration. De sammenlignede dette resultat med et kommercielt tilgængeligt bovint (ko) decellulariseret spongiløst knoglexenograft og observerede ikke signifikant større knogleregenerering. Holdet testede derefter knogletransplantatmaterialet i en præklinisk hundemodel for tandudtrækning for at forstå sårheling i tandskålen, hvor ekstraktionsskålen behandlet med knogletransplantatet viste forbedret knogledannelse ved 12 uger. På dette tidspunkt, som forventet, knogletransplantatet blev stort set erstattet af knoglevæv.
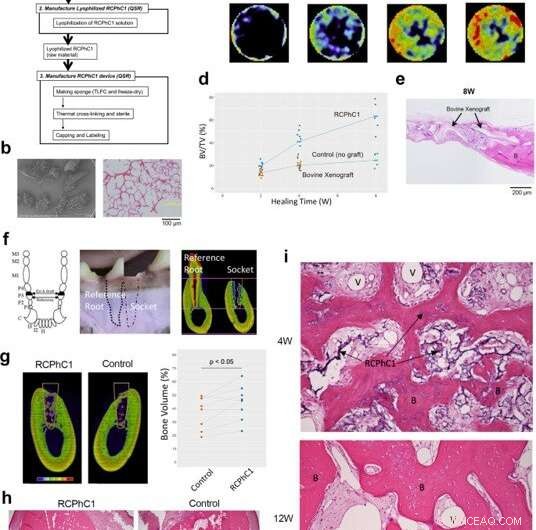
Præklinisk effektivitetstest af RCPhC1-materialet optimeret til knogletransplantation i gnaver- og hundemodeller. (a) Flowdiagram over RCPhC1-knogletransplantatfremstillingsprocessen. Skala bar er lig med 100 μm. (b) RCPhC1-knogletransplantat blev fremstillet som porøst granulat af størrelse 300-1200 µm for bedre håndtering. Skala bar er lig med 100 μm. (c) Tidsforløb for knogleregenerering induceret af RCPhC1-knogletransplantat i calvarial defektmodellen hos rotter. Histologisk analyse (øverste række) afslørede nydannet knoglevæv (B) i RCPhC1-transplantatmateriale, som blev resorberet over tid. En tidsforløbsserie af in vivo microCT (nederste række) viste den progressive stigning i knoglevæv. (d) Tidsforløb for BV/TV-måling af rotte calvarial knogledefekt implanteret med RCPhC1 knogletransplantat, bovin decellulariseret spongiløs knogle xenograft og ingen graft kontrol. (e) Histologisk evaluering af bovint xenograft implanteret i calvarial knogledefekt hos rotter. Den fysiske struktur af bovint xenotransplantat svarede til den for RCPhC1-knogletransplantat. I periferien af defekten, bovint xenograft blev set fusioneret til den nydannede knogle (B). I midten af defekten, okse xenograftgranulat var omgivet af fibrøst væv. Skala bar er lig med 200 μm. (f) Model for udtrækning af hundetand. Hundens tredje præmolar (P3) har næsten identiske mesiale og distale rødder. Den tredje præmolar blev hemi-sektioneret, og kun den distale rod blev ekstraheret. Den ene side af post-ekstraktionsbenet socket blev fyldt med RCPhC1, mens den anden side blev efterladt til at hele uden yderligere behandling. Den resterende mediale rod blev endodontisk behandlet og tjente som reference. Skalastangen svarer til 4 mm. (g) MicroCT-tværsnit, der viser knogleregenerering i ekstraktionsskålen (hvid linje) efter 12 ugers (12 W) heling. Knoglevolumenet i socket var signifikant større i den RCPhC1-knogletransplantatimplanterede socket end den ubehandlede kontrolsocket (n = 8; tosidet parret t-test). Skalastangen svarer til 4 mm. (h) Histologisk tværsnit af ekstraktionssokkelen (hvid linje) ved 12 W. Sokkelen, der modtog RCPhC1 knogletransplantat, udviste større knogleregenerering. Punkterede hvide linjer viser stikkontakter. Målestok er lig med 1 mm. (i) Histologisk evaluering af RCPhC1 knogletransplantat (I) associeret knogleregenerering. Rigelig vaskulær dannelse (II) i knoglemarvsvævet blev noteret for regenererende knogle (III) efter 4 ugers (4 W) heling. RCPhC1-knogletransplantat blev stort set resorberet efter 12 W heling. Den regenererede knogle indeholdt vitale osteocytter (IV). Kredit:Nature Communications Materials, doi:10.1038/s43246-020-00089-9
Udsigter for syntetiske stilladser i knoglevævsteknik
På denne måde Hideo Fushimi og kolleger optimeret en enkel, men kritisk ingeniørproces til at regulere koncentrationen af opløst stof af et rekombinant polypeptid af humant type I kollagen alpha I-kædeprotein med målrettede aminosyresubstitutioner, forkortet RCPhC1. Holdet implanterede først konstruktionen i en rotte-calvarial knogledefektmodel for at forstå de optimale tekniske faktorer til fremstilling af knogletransplantatet. De designede knogletransplantatmaterialet til at understøtte migrationen af mesenkymale stamceller (MSC'er) mod defektområdet og gav et stimulerende mikromiljø til osteogen differentiering. Knogletransplantatmaterialet alene viste et ideelt helingsmønster i fravær af vækstfaktorer og stamceller til at regenerere knogle. Materialet kan bruges til at generere vævsspecifikt medicinsk udstyr og graftstilladser med betydelig fremstillings-alsidighed inden for knoglevævsteknik.
© 2020 Science X Network
 Varme artikler
Varme artikler
-
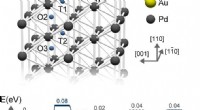 Hvorfor guld-palladium-legeringer er bedre end palladium til brintlagringAu-atomerne destabiliserer kemisorberet brint, dermed øge deres energi og reducere barrieren. Kredit:2018 Shohei Ogura, Institut for Industrividenskab, Universitetet i Tokyo Materialer, der absorb
Hvorfor guld-palladium-legeringer er bedre end palladium til brintlagringAu-atomerne destabiliserer kemisorberet brint, dermed øge deres energi og reducere barrieren. Kredit:2018 Shohei Ogura, Institut for Industrividenskab, Universitetet i Tokyo Materialer, der absorb -
 Opdagelse af bakteriel enzymaktivitet kan føre til nye sukkerbaserede lægemidlerKredit:Danmarks Tekniske Universitet Forskere fra DTU Biosustain og DTU Bioengineering har belyst aktiviteten af enzymet N-acetylgalactosaminidase (GH109), hvis aktivitetsmekanisme indtil nu har
Opdagelse af bakteriel enzymaktivitet kan føre til nye sukkerbaserede lægemidlerKredit:Danmarks Tekniske Universitet Forskere fra DTU Biosustain og DTU Bioengineering har belyst aktiviteten af enzymet N-acetylgalactosaminidase (GH109), hvis aktivitetsmekanisme indtil nu har -
 Rens gennem solenergiDemonstrator for en mobil målepistol med selvlysende polymerbærer. Kredit:Fraunhofer IST / Falko Oldenburg I kombination med de rigtige materialer, solstråler kan gøre underværker:de renser bygnin
Rens gennem solenergiDemonstrator for en mobil målepistol med selvlysende polymerbærer. Kredit:Fraunhofer IST / Falko Oldenburg I kombination med de rigtige materialer, solstråler kan gøre underværker:de renser bygnin -
 3-D-printede væv kan holde atleter i aktionRice University-studerende Sean Bittner har en prøve af et 3D-printet stillads, der en dag kan hjælpe med at helbrede osteochondrale skader af den slags, som atleter ofte lider af. Materialet efterlig
3-D-printede væv kan holde atleter i aktionRice University-studerende Sean Bittner har en prøve af et 3D-printet stillads, der en dag kan hjælpe med at helbrede osteochondrale skader af den slags, som atleter ofte lider af. Materialet efterlig
- NASA finder en mindre langstrakt potentiel Tropical Cyclone Six
- Ny forskning viser, at væksten i det østlige antarktiske islag var mindre end tidligere foreslået
- Nye lithium batterier fra brugte mobiltelefoner
- En økonomisk legeringsbaseret aerogel som elektrokatalysator til carbonfiksering
- Fjern galakse udsender 15 højenergi-radioudbrud
- Fysikere scorer dobbelt hit i LED-forskning


