Saltopløsning i vand:Forstå processen og opløsningen
* Dissociation: De ioniske bindinger, der holder natrium (Na+) og chlorid (Cl-) ioner sammen i saltkrystallen bryder.
* Hydrering: Vandmolekylerne omgiver de individuelle ioner og danner en hydreringsskal. Den positive ende af et vandmolekyle (brint) tiltrækkes af de negativt ladede chloridioner, mens den negative ende (ilt) tiltrækkes af de positivt ladede natriumioner.
* Løsning: De hydrerede ioner er nu spredt jævnt i vandet, hvilket skaber en homogen blanding kaldet en saltvandsopløsning.
Vigtig bemærkning: Selve saltet forsvinder ikke. Det nedbrydes bare til dets bestanddele, som derefter er omgivet af vandmolekyler. Du kan få saltet tilbage ved at fordampe vandet.
Sidste artikelHalogener:Forståelse af metalloider og deres fravær
Næste artikelHydrogenoxid (vand) som en kovalent forbindelse:Forklaret
 Varme artikler
Varme artikler
-
 Polyethylen:Grundlaget for moderne plastikPolyethylen:Grundlaget for moderne plastik Plast er allestedsnærværende i nutidens liv, hvor polyethylen tegner sig for den største andel af den globale plastikproduktion. Al plast er polymerer samme
Polyethylen:Grundlaget for moderne plastikPolyethylen:Grundlaget for moderne plastik Plast er allestedsnærværende i nutidens liv, hvor polyethylen tegner sig for den største andel af den globale plastikproduktion. Al plast er polymerer samme -
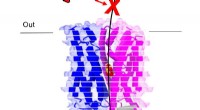 Forskere opdager, hvordan malariaparasitter importerer sukkerStruktur af transportproteinet PfHT1 i kompleks med sukker D-glucose. Kredit:David Drew Forbruget af sukker er en grundlæggende kilde til brændstof i de fleste levende organismer. I malariaparasit
Forskere opdager, hvordan malariaparasitter importerer sukkerStruktur af transportproteinet PfHT1 i kompleks med sukker D-glucose. Kredit:David Drew Forbruget af sukker er en grundlæggende kilde til brændstof i de fleste levende organismer. I malariaparasit -
 Pulverisering af elektronisk affald er grønt, ren - og koldPrintplader fra elektronik, som computermus, kan knuses til nanodstøv af en kryomølle, ifølge forskere ved Rice University og Indian Institute of Science. Støvet kan derefter let adskilles i dets komp
Pulverisering af elektronisk affald er grønt, ren - og koldPrintplader fra elektronik, som computermus, kan knuses til nanodstøv af en kryomølle, ifølge forskere ved Rice University og Indian Institute of Science. Støvet kan derefter let adskilles i dets komp -
 Overvågning af smeltet stål med laser - ståleksperter kan spare industrien millionerDr. Szymon Kubal afbilledet med et kar af smeltet stål på Tata Steel Port Talbot-værket. Kredit:Tata Steel Stålarbejdere vil i realtid kunne overvåge temperaturen og den kemiske sammensætning i sm
Overvågning af smeltet stål med laser - ståleksperter kan spare industrien millionerDr. Szymon Kubal afbilledet med et kar af smeltet stål på Tata Steel Port Talbot-værket. Kredit:Tata Steel Stålarbejdere vil i realtid kunne overvåge temperaturen og den kemiske sammensætning i sm
- Den indiske IT-gigant TCSs overskud stiger med 24 procent
- Forsker udforsker at bruge nanopartikler til at reducere størrelsen af dybtliggende tumorer
- Bilister i Cairo udsat for farlige niveauer af forurening, ny undersøgelse finder
- Hvad bruger celler til at udføre aktiv transport?
- De indre farvande er en blind plet i udledningen af drivhusgasser
- Hvad er ATP's rolle i menneskets krop?


